Cho 1,68 gam MgCO3 tác dụng với một lượng vừa đủ dung dịch HCl 2M. Thể tích dung dịch HCl đã dùng là (cho Mg=24, C=12, O=16)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


MgCO3+2HCl->MgCl2+H2O+CO2
0,25--------0,5
n MgCO3=\(\dfrac{21}{84}\)=0,25 mol
=>VHCl=\(\dfrac{0,5}{2}\)=0,25 l=250ml
=>B

28.
\(n_{MgCO_3}=\dfrac{4,2}{84}=0,05(mol)\\ MgCO_3+2HCl\to MgCl_2+H_2O+CO_2\uparrow\\ \Rightarrow n_{HCl}=0,1(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,1}{2}=0,05(l)\)
29.
\(Zn+H_2SO_4\to ZnSO_4+H_2\\ \Rightarrow n_{Zn}=n_{H_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ \Rightarrow \%_{Zn}=\dfrac{0,1.65}{10,5}.100\%=62\%\\ \Rightarrow \%_{Cu}=100\%-62\%=38\%\)
30.
Đặt KL là R
\(n_{HCl}=2.0,1=0,2(mol)\\ 2R+O_2\xrightarrow{t^o}2RO\\ RO+2HCl\to RCl_2+H_2O\\ \Rightarrow n_RO=0,1(mol)\\ \Rightarrow M_RO=\dfrac{4}{0,1}=40(g/mol)\\ \Rightarrow M_R=40-16=24(g/mol)(Mg)\)
bạn ơi v câu 30 đáp án là câu nào vậy mình ko hiểu lắm

Fe+2HCl->FeCl2+H2
x---2x-----------x
Mg+2HCl->MgCl2+H2
y------2y-----------y
Ta có :
\(\left\{{}\begin{matrix}56x+24y=24\\x+y=\dfrac{13,44}{22,4}\end{matrix}\right.\)
=>x=0,3 mol, y=0,3 mol
=>%m Fe=\(\dfrac{0,3.56}{24}.100\)=70%
=>%m Mg=100-70=30%
=>VHCl=\(\dfrac{0,3.2+0,3.2}{2}\)=0,6l=600ml
b)
XCl2+2AgNO3->2AgCl+X(NO3)2
0,6--------------------1,2mol
=>m AgCl=1,2.143,5=172,2g

1:
a) \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
______0,2------>0,2------------------->0,2_____(mol)
=> \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b) \(V_{ddH_2SO_4}=\dfrac{0,2}{1}=0,2\left(l\right)\)
2:
a)
\(n_{HCl}=2.0,2=0,4\left(mol\right)\)
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
______0,2<------0,4------------------>0,2______(mol)
=> \(m_{Mg}=0,2.24=4,8\left(g\right)\)
b) \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)

a, Ta có: \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Theo PT: \(n_{H_2}=n_{Mg}=0,2\left(mol\right)\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, \(n_{HCl}=2n_{Mg}=0,4\left(mol\right)\Rightarrow C\%_{HCl}=\dfrac{0,4.36,5}{100}.100\%=14,6\%\)
Để giải bài toán này, ta cần viết phương trình phản ứng giữa Mg và HCl:
$$\text{Mg} + 2\text{HCl} \rightarrow \text{MgCl}2 + \text{H}2$$
Theo đó, 1 mol Mg tác dụng với 2 mol HCl để tạo ra 1 mol H2. Ta có thể tính số mol Mg trong 4,8g Mg như sau:
$$n{\text{Mg}} = \frac{m{\text{Mg}}}{M_{\text{Mg}}} = \frac{4,8}{24} = 0,2 \text{mol}$$
Vì 1 mol Mg tác dụng với 2 mol HCl để tạo ra 1 mol H2, nên số mol HCl cần để tác dụng với 0,2 mol Mg là 0,4 mol. Từ đó, ta có thể tính khối lượng HCl cần dùng như sau:
$$m_{\text{HCl}} = n_{\text{HCl}} \times M_{\text{HCl}} = 0,4 \times 36,5 = 14,6 \text{g}$$
Vậy, dung dịch HCl có nồng độ $c = \frac{m_{\text{HCl}}}{V_{\text{HCl}}}$, trong đó $V_{\text{HCl}}$ là thể tích dung dịch HCl đã dùng. Để tính thể tích HCl đã dùng, ta cần biết nồng độ của dung dịch axit HCl đã dùng. Ta có thể tính nồng độ % của dung dịch axit HCl như sau:
$$\text{nồng độ %} = \frac{m_{\text{HCl}}}{m_{\text{dung dịch}}} \times 100%$$
Trong đó, $m_{\text{dung dịch}}$ là khối lượng của dung dịch HCl đã dùng. Từ đó, ta có thể tính được thể tích dung dịch HCl đã dùng và thể tích H2 thoát ra ở đktc như sau:
\begin{align*}
m_{\text{dung dịch}} &= \frac{m_{\text{HCl}}}{\text{nồng độ %}} = \frac{14,6}{36,5} \times 100% = 40\text{g} \
V_{\text{HCl}} &= \frac{m_{\text{HCl}}}{c_{\text{HCl}}} = \frac{14,6}{0,365} = 40\text{mL} \
V_{\text{H}2} &= n{\text{H}2} \times V{\text{m}} = 0,1 \times 24,45 = 2,445\text{L}
\end{align*}
Vậy, thể tích H2 thoát ra ở đktc là 2,445 L.

PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
Ta có: \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,2\left(mol\right)\\n_{H_2}=0,1\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C\%_{HCl}=\dfrac{0,2\cdot36,5}{200}\cdot100\%=3,65\%\\V_{H_2}=0,1\cdot22,4=2,24\left(l\right)\end{matrix}\right.\)
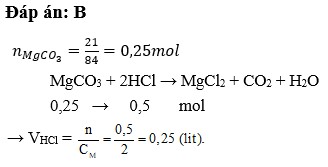
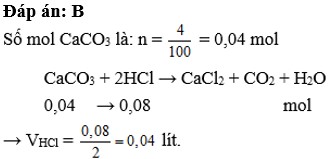
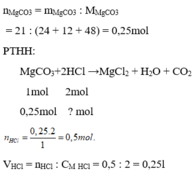
\(n_{MgCO_3}=\dfrac{1,68}{84}=0,02\left(mol\right)\)
PTHH: MgCO3 + 2HCl --> MgCl2 + CO2 + H2O
______0,02--->0,04
=> \(V_{ddHCl}=\dfrac{0,04}{2}=0,02\left(l\right)\)