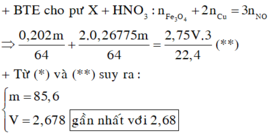một hỗn hợp gồm 2 kim loại X và Y (X có hoá trị II, Y có hoá trị III trong hợp chất). Lấy 20,7 gam hỗn
hợp cho tác dụng với O2 dư thu được 37,5 gam hỗn hợp oxit.
a. Cho 20,7 gam hỗn hợp trên tác dụng với axit HCl thì thu được bao nhiêu lit H2 (đktc)
b. Tìm 2 kim loại X, Y biết trong hỗn hợp oxit, tỉ lệ mol là 6:5 và trong oxit kim loại X, Y chiếm
52,94% khối lượng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
+ n F e 3 O 4 = n O 4 = m - 0 , 798 m 16 . 4 = 0 , 202 m 64 n C u = m - 232 . 0 , 202 m 64 64 = 0 , 26775 m 64 → H C l d ư F e C l 2 : 0 , 606 m / 64 C u C l 2 : 0 , 202 m / 64 H C l d ư ⏟ Y + C u ⏟ Z + Y + A g N O 3 d ư → N O ↑ + A g C l ↓ A g ↓ ⇒ n A g C l = 2 n F e C l 2 + 2 n C u C l 2 + n H C l = 2 n F e C l 2 + 2 n C u C l 2 + 4 n N O = 1 , 616 m 64 + 4 V 22 , 4 n F e 2 + = 3 n N O + n A g ⇔ 0 , 606 m 64 = 3 V 22 , 4 + 427 , 44 - 143 , 5 1 , 616 m 64 + 4 V 22 , 4 108 ( * ) + B T E c h o p ư X + H N O 3 : n F e 3 O 4 + 2 n C u = 3 n N O ⇒ 0 , 202 m 64 + 2 . 0 , 26775 m 64 = 2 , 75 V . 3 22 , 4 ( * * ) + T ừ ( * ) v à o ( * * ) s u y r a : m = 85 , 6 V = 2 , 678 g ầ n n h ấ t v ớ i 2 , 68

Đáp án D
Có

m g X + HNO3 đặc nguội → 0,1 mol NO2
→ BTe a . n M = 0 , 1 m o l ( 2 )
Từ (1) và (2) suy ra:
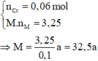
=> a = 2, M = 65 (M là Zn).

Câu 11 :
Gọi $n_{CuO} = a(mol) ; n_{Fe_2O_3} = b(mol)$
$\Rightarrow 80a + 160b = 20(1)$
$CuO + 2HCl \to CuCl_2 + H_2O$
$Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O$
Theo PTHH :
$n_{HCl} = 2a + 6b = 0,2.3,5 = 0,7(2)$
Từ (1)(2) suy ra a= 0,05 ; b = 0,1
Ta có :
$\%m_{CuO} = \dfrac{0,05.80}{20}.100\% = 20\%$
$\%m_{Fe_2O_3} = 100\% -20\% = 80\%$
Đáp án B

Số OXH của Fe sau khi tác dụng với dung dịch HCl là +2 còn sau khi td với Cl2 là +3
TN1
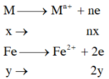
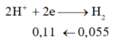
=> nx+2y=0,11 (1)
TN2: Xét cả quá trình
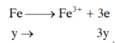
=> nx+3y=0,12 (2)
(1)-(2) được y=0,01
Thay y=0,01 vào (2) được nx=0,09(3)
Lại có: 56.0,01+ xM=1,37
=> Mx=0,81 (4)
(3)(4)=> M=9n
=> Kim loại là Al
Đáp án C

Đáp án A
m X = 136a => m O = 11,36 => n O = 0,71 mol
Quy đổi hỗn hợp X về a mol Mg, 2a mol Fe và 0,71 mol O.
Y tác dụng với HNO3 dư tạo ra khí NO, N2O và dung dịch chứa muối NH4NO3.
Cô cạn dung dịch thu được rắn chứa a mol Mg(NO3)2 , 2a mol Fe(NO3)3 và NH4NO3.
→ n N H 4 N O 3 = 0 , 1875 a
Do vậy số mol NO và N2O đều là 0,1875a.
Bảo toàn e: 2a + 2a.3 = 0,71.2 + 0,1875a.3 + 0,1875a.8 + 0,1875a.8
Giải được: a=0,32.
Đốt hỗn hợp X bắng Cl2 và O2 thu được Z.
Hòa tan Z cần 1,6 mol HCl → n O = 0 , 8 → n O 2 = 0 , 4
Gọi số mol Cl2 là x , kết tủa thu được là AgCl 2x +1,6 và Ag.
Bảo toàn e: n A g = 0,32.2 + 0,64.3 - 0,8.2 - 2x = 0,06 - 2x
=> 108(0,96 - 2x) + (108 + 35,5)(2x + 16) = 354,8
Giải được: x=0,3.
=> V = (0,3 + 0,4).22,4 = 15,68