Hai nguyên tố X, Y (MX< MY) thuộc nhóm IIA, ở hai chu kì liên tiếp nhau trong bảng tuần hoàn các nguyên tố hoá học. Biết 4,4 gam hỗn hợp X và Y phản ứng hoàn toàn với lượng dư dung dịch HCl, thu được 3,36 lít H2 (đktc). Xác định các nguyên tố X, Y.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{HCl}=\dfrac{219.10}{100.36,5}=0,6\left(mol\right)\)
ACO3 + 2HCl --> ACl2 + CO2 + H2O
BCO3 + 2HCl --> BCl2 + CO2 + H2O
=> nHCl = 2.nCO2 = 2.nH2O
=> nCO2 = nH2O = 0,3 (mol)
Theo ĐLBTKL: mhh ban đầu + mHCl = mhh muối clorua + mCO2 + mH2O
=> mhh muối clorua = 26,8 + 0,6.36,5 - 0,3.44 - 0,3.18 = 30,1 (g)

NaX + AgNO 3 → NaNO 3 + AgX
a mol a mol a mol a mol
NaY + AgNO 3 → NaNO 3 + AgY
b mol b moi b mol b mol
n AgNO 3 = 0,2 x 150/1000 = 0,O3 mol
m AgNO 3 = 0,3 x 170 = 5,1g
n NaNO 3 = 0,O3 => m NaNO 3 = 0,03 x 85 = 2,55g
Áp dụng định luật bảo toàn khối lượng, ta có :
2,2 + 5,1 = 2,55 + m kết tủa → m kết tủa = 4,75 (gam)
(108 + X)a + (108 + Y)b = 4,75 ; a + b = 0,O3 (mol)
Xa + Yb + 15,1. Cho X > Y ; Xa + Xb > Xa + Yb > Ya + Yb
X > 1,51/0,03 > Y > X > 50,3 > Y
X và Y là các halogen liên tiếp, vậy đó là brom (80) và Cl (35,5).

Đáp án : A
m gam X phản ứng với HCl tạo lượng khí lớn hơn khi phản ứng với H2O
=> Trong X có kim loại không phản ứng với H2O
Mà Y và Z thuộc 2 chu kỳ liên tiếp => Y là Mg(24) và Z là Ca(40)
Do nCa = nH2(1) = V 22 , 4 mol và nMg = nH2(2) – nCa = 2. V 22 , 4
=> Hỗn hợp kim loại có tỷ lệ mol Mg:Ca là 2:1
=> %mY(X) = 54,54%
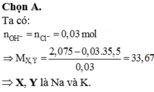

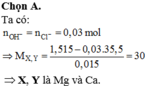




Gọi công thức chung của hai kim loại là M = a mol
M + 2HCl ->> MCl2 + H2
(mol): a 2a a
Số mol H2 = 0,15 mol nên a = 0,15 mol
Ta có: MX = 4,4 -> M = 29,33 đvC
Xvà Ylà 2 kim loại nằm ở 2 chu kỳ liên tiếp thuộc nhóm IIA nên X là Mg và Y là Ca
pp chủ tus , treo máy nghỉ đây, nếu còn hỏi thì chiều hỏi nhé