Một hỗn hợp gồm 2 ankan X và Y là đồng đẳng kế tiếp nhau có khối lượng 10,2 gam.Đốt cháy hoàn toàn hỗn hợp cần 36,8 gam O2. Tìm CTPT của 2 ankan, Tính % khối lượng mỗi ankan trong hỗn hợp?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi công thức chung của X, Y là CnH2n+2
\(n_{O_2}=\dfrac{36,8}{32}=1,15\left(mol\right)\)
PTHH: CnH2n+2 + \(\dfrac{3n+1}{2}\)O2 --to--> nCO2 + (n+1)H2O
\(\dfrac{2,3}{3n+1}\)<-----1,15
=> \(M_{C_nH_{2n+2}}=14n+2=\dfrac{10,2}{\dfrac{2,3}{3n+1}}\left(g/mol\right)\)
=> n = 3,5
Mà X,Y là 2 ankan kế tiếp nhau
=> X, Y là C3H8 và C4H10
Gọi số mol C3H8 và C4H10 là a, b (mol)
PTHH: C3H8 + 5O2 --to--> 3CO2 + 4H2O
a--->5a---------->3a----->4a
2C4H10 + 13O2 --to--> 8CO2 + 10H2O
b------->6,5b--------->4b------>5b
=> \(\left\{{}\begin{matrix}44a+58b=10,2\\5a+6,5b=1,15\end{matrix}\right.\)
=> a = 0,1; b = 0,1
=> \(\left\{{}\begin{matrix}m_{C_3H_8}=0,1.44=4,4\left(g\right)\\m_{C_4H_{10}}=0,1.58=5,8\left(g\right)\end{matrix}\right.\)
\(n_{CO_2}=3a+4b=0,7\left(mol\right)\)
=> \(m_{CO_2}=0,7.44=30,8\left(g\right)\)
\(m_{H_2O}=\left(4a+5b\right).18=16,2\left(g\right)\)

Dùng pp bảo toàn nguyên tố Oxi và bảo toàn khối lượng.
Gọi a = n(CO2) ; b = n(H2O).
Ta có: 44a + 18b = m(ankan) + m(O2) = 47 (g).
Áp dụng BT nguyên tố Oxi:
2a + b = 36,8/32 * 2 = 2,3.
Giải hệ 2 pt trên tìm được a = 0,7 ; b = 0,9.
==> m(CO2) = 30,8 (g) ; m(H2O) = 16,2 (g).

Gọi công thức chung của 2 ankan trong A : \(C_nH_{2n+2}\)
PTHH: \(C_nH_{2n+2}+\dfrac{3n+1}{2}O_2\rightarrow nCO_2+\left(n+1\right)H_2O\)
\(n_{O_2}=\dfrac{36,8}{32}=1,15\left(mol\right)\)
Theo PT ta có : \(n_{C_nH_{2n+2}}=1,15:\dfrac{3n+1}{2}\left(mol\right)\)
=> \(\dfrac{10,2}{14n+2}=1,15:\dfrac{3n+1}{2}\)
=> n=3,5
=> nhhakan = \(\dfrac{10,2}{14.3,5+2}=0,2\left(mol\right)\)
Vì hỗn hợp A gồm 2 ankan là đồng đẳng kế tiếp.
=> 2 ankan cần tìm là C3H8 và C4H10
Gọi x, y lần lượt là số mol của C3H8 và C4H10
=> \(\left\{{}\begin{matrix}x+y=0,2\\44x+58y=10,2\end{matrix}\right.\)
=> x=0,1 , y=0,1
Vì thành phần phần trăm thể tích trong A cũng là thành phần phần trăm số mol trong A.
=> \(\%V_{C_3H_8}=\dfrac{0,1}{0,2}.100=50\%\)
\(\%V_{C_4H_{10}}=\dfrac{0,1}{0,2}.100=50\%\)

CTTQ của ankan : \(C_nH_{2n+2}\)
\(n_{O_2} = \dfrac{2,24.2}{0,082.(0+273)} = 0,2(mol)\\ C_nH_{2n+2} + \dfrac{3n+1}{2}O_2 \xrightarrow{t^o} nCO_2 + (n+1)H_2O\\ n_{ankan} = \dfrac{2}{3n+1}n_{O_2} = \dfrac{0,4}{3n+1}(mol)\\ \Rightarrow \dfrac{0,4}{3n+1}.(14n+2) = 1,76\\ \Rightarrow n = 3\)
Vậy CTPT hai ankan là : \(C_2H_6,C_4H_{10}\)

a) \(n_{O_2}=\dfrac{21,056}{22,4}=0,94\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{52}{100}=0,52\left(mol\right)\)
BTNT C: \(n_C=n_{CO_2}=n_{CaCO_3}=0,52\left(mol\right)\)
BTNT O: \(n_{H_2O}=2n_{O_2}-2n_{CO_2}=0,84\left(mol\right)\)
\(\Rightarrow n_{ankan}=n_{H_2O}-n_{CO_2}=0,32\left(mol\right)\)
\(\Rightarrow\text{Số }\overline{C}_{\text{trung bình}}=\dfrac{n_C}{n_{ankan}}=\dfrac{0,52}{0,32}=1,625\)
Vì 2 ankan liên tiếp nhau trong dãy đồng đẳng nên 2 ankan là CH4 (metan) và C2H6 (etan)
b) BTNT H: \(n_H=2n_{H_2O}=1,68\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_6}=b\left(mol\right)\end{matrix}\right.\left(a,b>0\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_C=n_{CH_4}+2n_{C_2H_6}=a+2b=0,52\\n_H=4n_{CH_4}+6n_{C_2H_6}=4a+6b=1,68\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,12\\b=0,2\end{matrix}\right.\left(TM\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{0,12.16}{0,12.16+0,2.30}.100\%=24,24\%\\\%m_{C_2H_6}=100\%-24,24\%=75,76\%\end{matrix}\right.\)
c)
\(CH_4+Cl_2\xrightarrow[]{askt}CH_3Cl\left(\text{metyl clorua}\right)+HCl\\ C_2H_6+Cl_2\xrightarrow[]{askt}C_2H_5Cl\left(\text{etyl clorua}\right)+HCl\)

Đáp án A
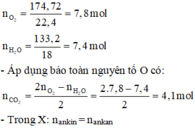
=> Quy đổi X tương đương với hỗn hợp chỉ gồm anken và amin no, đơn chức, mạch hở.

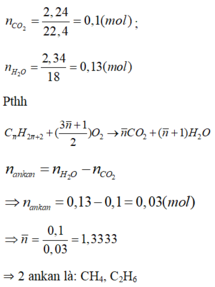
\(CT:C_{\overline{n}}H_{2\overline{n}+2}\)
\(n_{O_2}=\dfrac{36.8}{32}=1.15\left(mol\right)\)
\(\)\(C_{\overline{n}}H_{2\overline{n}+2}+\dfrac{3\overline{n}+1}{2}O_2\underrightarrow{t^0}nCO_2+\left(n+1\right)H_2O\)
\(\dfrac{2.3}{3\overline{n}+1}........1.15\)
\(M=\dfrac{10.2}{\dfrac{2.3}{3\overline{n}+1}}=\dfrac{102}{23}\left(3\overline{n}+1\right)\)
\(\Rightarrow14\overline{n}+2=\dfrac{102}{23}\cdot\left(3\overline{n}+1\right)\)
\(\Rightarrow\overline{n}=3.5\)
\(CT:C_3H_8\left(amol\right),C_4H_{10}\left(bmol\right)\)
\(m=44a+58b=10.2\left(g\right)\left(1\right)\)
\(n_{O_2}=5a+6.5b=1.15\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(a=b=0.1\)
\(\%C_3H_8=\dfrac{4.4}{10.2}\cdot100\%=43.13\%\)
\(\%C_4H_{10}=56.84\%\)