Để trung hòa hết 40,5 gam dung dịch HX (X: F, Cl, Br, I) nồng độ 10% người ta phải dùng dung dịch AgNO3 dư thu được 8,5 gam kết tủa. Dung dịch axit ở trên là dung dịch
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Áp dụng phương pháp tăng giảm khối lượng:
Cứ 1 mol MCl2 → 1 mol M(NO3)2 và 2 mol AgCl thì m tăng 2.62 - 2.35,5 = 53 gam
Phản ứng tạo 0,12 mol AgCl có khối lượng muối tăng 3,18 gam
mmuối nitrat = mmuối clorua + mtăng = 5,94 + 3,18 = 9,12 (gam)
Đáp án C

a) 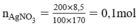
Phương trình hóa học của phản ứng:
HCl + AgNO3 → AgCl + HNO3
Theo pt nHCl = nAgCl = 0,1 mol
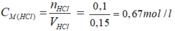
b) 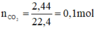
Phương trình hóa học của phản ứng:
HCl + NaHCO3 → NaCl + CO2↑ + H2O
Theo pt: nHCl = nCO2 = 0,1 mol ⇒ mHCl = 0,1. 36,5 = 3,65 g
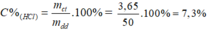

Bài 6 :
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
x ___________x _______x
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
y ____________y_______ y
\(n_{H2}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
\(\rightarrow x+y=0,25\left(1\right)\)
\(2NaOH+FeCl_2\rightarrow Fe\left(OH\right)_2+2NaCl\)
__________ x ______ x
\(2NaOH+MgCl_2\rightarrow Mg\left(OH\right)_2+2NaCl\)
__________y _________ y
Ta có mFe(OH)2+mMg(OH)2=17,7
\(\rightarrow90x+58y=17,1\left(2\right)\)
(1)(2)\(\rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,15\end{matrix}\right.\)
\(\rightarrow m_{Fe}=0,1.56=5,6\left(g\right);m_{Al}=0,15.27=4,05\left(g\right)\)
\(2Fe+3Cl_2\rightarrow2FeCl_3\)
0,1____0,15
\(Mg+Cl_2\rightarrow MgCl_2\)
0,15__0,15
\(V_{Cl2}=0,3.22,4=6,72\left(l\right)\)
Bài 2 :
\(n_{HBr}=\frac{1}{81},n_{NaOH}=\frac{1}{40}\)
\(n_{NaOH}>n_{HBr}\rightarrow\) Chuyển xanh
Bài 3 :
\(m\downarrow=m_{AgCl}=0,1.143,5=14,35\left(g\right)\)
Bài 4 :
\(m_{HX}=29,2\left(g\right)\rightarrow n_{HX}=\frac{29,2}{X+1}\left(mol\right)\)
\(n_{NaOH}=0,8\left(mol\right)=n_{HX}\)
\(\rightarrow\frac{29,2}{X+1}=0,8\Leftrightarrow X=35,5\left(Cl\right)\)
Vậy HX là HCl
Bài 5 :
a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
__a____________a________a
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
b_____________b_________b
\(\rightarrow a+b=0,25\left(1\right)\)
\(FeCl_2+2NaOH\rightarrow Fe\left(OH\right)_2\downarrow+2NaCl\)
a_________________a____________________
\(MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2+2NaCl\)
b___________________b_________________
\(m_{kettua}=17,7\left(g\right)\rightarrow90a+58b=17,7\left(2\right)\)
(1);(2) \(\rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,15\end{matrix}\right.\)
\(n_{Fe}=0,1\left(mol\right)\rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
\(n_{Mg}=0,15\left(mol\right)\rightarrow m_{Mg}=0,15.24=3,6\left(g\right)\)
b, \(2Fe+3Cl_2\underrightarrow{^{to}}2FeCl_3\)
0,1_____0,15_____________
\(Mg+Cl_2\underrightarrow{^{to}}MgCl_2\)
0,1___0,1__________
\(\rightarrow n_{Cl2}=0,15+0,1=0,25\left(mol\right)\)
\(\rightarrow V_{Cl2}=0,25.22,4=5,6\left(l\right)\)

Đáp án A
Ag++ Cl- →AgCl
nCl- = nAg+ = 0,07 mol (trong 10 ml A)
Gọi số mol Cu2+; Fe3+ có trong 100 ml A là x, y mol
Theo ĐLBT ĐT thì: 2x+ 3y = 0,7
64x+ 56y+ 0,7.35,5 = 43,25 gam
Suy ra x = 0,2; y = 0,1
Suy ra nồng độ mol các ion Cu2+,Fe3+,Cl- lần lượt là 2M; 1M; 7M
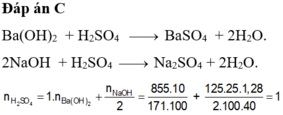
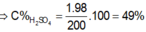
\(AgNO_3 + HX \to AgX + HNO_3\\ n_{AgX} = n_{HX}\\ \Rightarrow \dfrac{8,5}{108+X} = \dfrac{40,5.10\%}{1+X}\\ \Rightarrow X = 96,38\)
(Sai đề)