Ngâm một đinh sắt vào dung dịch CuSO4 2M. Sau một thời gian nhấc đinh sắt ra rửa nhẹ, làm khô cân thấy khối lượng đing sắt tăng 0,2 gam. Tính khối lượng sắt phản ứng và khối lượng đồng bám trên đinh sắt.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đặt nFe(pứ)=a(mol)
PTHH Fe +CuSO4------>FeSO4+Cu
Theo phương trình =>nFe=nCu=a(mol)
mđinh sắt tăng=mcu-mFe=64a-56a=0,2(g)
=>a=0,025(mol)
=>mFe(pứ)=0,025.56=1,4(g)
mCu=0,025.64=1,6(g)

Tham khảo:
PTHH: Fe + CuSo4 ---->FeSo4 + Cu
Gọi a(mol) là số mol của Fe phản ứng
mCu - mFe = 3.5 - 2.3 = 1.2(g)
<--> 64a - 56a = 1.2
<--> 8a = 1.2
<--> a = 0.15
Dựa vào PTHH: nFe = nFeSo4 = 0.15(mol)
--> mFeSo4 = 0.15×152 = 22.8(g)

\(n_{Fe}=a\left(mol\right)\)
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
\(a............................a\)
\(m_{tăng}=m_{Cu}-m_{Fe}=64a-56a=51-50=1\left(g\right)\)
\(\Rightarrow a=0.125\left(mol\right)\)
\(m_{Fe}=0.125\cdot56=7\left(g\right)\)
\(m_{Cu}=0.125\cdot64=8\left(g\right)\)
\(m_{Fe\left(dư\right)}=50-7=43\left(g\right)\)

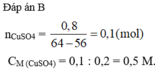
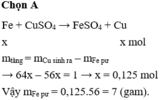
PTHH: Fe + CuSO4 --> FeSO4 + Cu
______a------------------------------>a
=> 64a - 56a = 0,2
=> 0,025 (mol)
=> mFe(pư) = 0,025.56 = 1,4 (g)
=> mCu = 0,025.64 = 1,6 (g)