Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(M_X = 18.2 = 36(đvC)\)
X gồm CO2,CO
Ta có :
\(44n_{CO_2} + 28n_{CO} = 36(n_{CO_2} + n_{CO})\\ \Rightarrow 8n_{CO_2} = 8n_{CO}\\ \Rightarrow n_{CO_2} = n_{CO}\)
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\)
Theo PTHH :
\(n_{CO} = n_{CO_2} = n_{CaCO_3} = \dfrac{20}{100} = 0,2(mol)\)
\(C + O_2 \xrightarrow{t^o} CO_2\\ 2C + O_2 \xrightarrow{t^o} 2CO\\ n_{O_2} = n_{CO_2} + \dfrac{n_{CO}}{2} = 0,3(mol)\\ \Rightarrow V = 0,3.22,4 = 6,72(lít)\)
\(\)

Đáp án B
2,3- dihidroxi propanal → CH2OH−CHOH−CHO hay C3H6O3
metyl fomiat: HCOOCH3 hay C2H4O2
fructozơ C6H12O6
andehit fomic: HCHO hay CH2O
so sánh thấy tỉ lệ số C : H : O = 1 : 2 : 1


Đáp án B
2,3- dihidroxi propanal → CH2OH−CHOH−CHO hay C3H6O3
metyl fomiat: HCOOCH3 hay C2H4O2
fructozơ C6H12O6
andehit fomic: HCHO hay CH2O
so sánh thấy tỉ lệ số C : H : O = 1 : 2 : 1
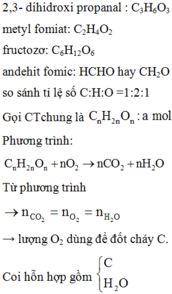
→ gọi công thức chung là C n H 2 n O n : a mol
Phương trình: C n H 2 n O n + nO 2 → nCO 2 + nH 2 O
Từ phương trình n CO 2 = n H 2 O = n O 2
→ lượng O2 dùng để đốt cháy C.
Coi hỗn hợp gồm C H 2 O
Như vậy:
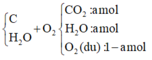
![]()
![]()


Đáp án A
Gọi x, y, z, t lần lượt là số mol của C3H6, C4H10, C2H2 và H2 trong m gam X.
Do Y có phản ứng với dung dịch brom nên H2 hết, ta có:
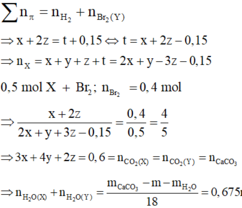
mX = mY = mC +mH = 8,55 gam
Theo định luật bảo toàn nguyên tố, ta có:
![]()

MX = 48 → nX = 0,96/48 = 0,02
Ta có:
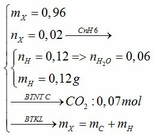
CO2 + Ba(OH)2 → BaCO3 + H2O
0,05 ←0,05 → 0,05
CO2 + BaCO3 + H2O → Ba(HCO3)2
0,02→ 0,02
Dư: 0,03
→ nBaCO3 dư = 0,03 → x = 5,91 (g) và mdd giảm = mBaCO3 – mCO2 + mH2O= 1,75 (g)

Đáp án A
Sử dụng sơ đồ đường chéo, ta có :
n C 4 H 4 ban đầu n H 2 ban đầu = 32 - 2 52 - 32 = 3 2 = 3 x 2 x
Gọi a là số mol H 2 phản ứng. Theo sự bảo toàn số liên kết π , bảo toàn C và sự tăng giảm số mol khí, ta có :
3 n C 4 H 4 ⏟ 3 x = n Br 2 phản ứng ⏟ 0 , 16 + n H 2 phản ứng ⏟ a n Y = 3 x ⏟ n C 4 H y - + ( 2 x - a ) ⏟ n H 2 dư = 1 , 792 22 , 4 = 0 , 08
⇒ 9 x = 0 , 16 + a 5 x - a = 0 , 08 ⇒ x = 0 , 02 a = 0 , 02
Đốt cháy hỗn hợp Y cũng chính là đốt cháy hỗn hợp X. Theo bảo toàn electron, ta có :
4 n O 2 ⏟ ? = 20 n C 4 H 4 ⏟ 0 , 02 . 3 + 2 n H 2 ⏟ 0 , 02 . 2
⇒ n O 2 = 0,32
⇒ V khong khi ( đktc ) = 0,32.5.22,4 = 35,84 lit




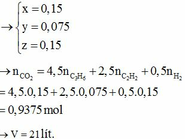
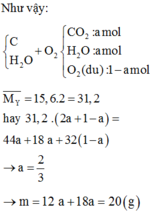

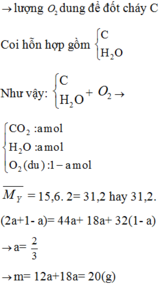
Đặt :
nCO = a (mol)
nCO2 = b (mol)
=> a + b = 0.4 (1)
mX = 28a + 44b = 40(a+b) (g)
=> 12a -4b = 0 (2)
(1) , (2):
a = 0.1
b = 0.3
mC = ( 0.1 + 0.3) * 12 = 4.8(g)
X gồm : CO2(x mol) ; CO(y mol)
Ta có :
\(n_X = x + y = \dfrac{8,96}{22,4} = 0,4\ mol\\ C + O_2 \xrightarrow{t^o} CO_2\\ 2C + O_2 \xrightarrow{t^o} 2CO\\ n_C = n_{CO_2} +n_{CO} = x + y = 0,3 + 0,1 = 0,4(mol)\\ \Rightarrow m = 0,4.12 = 4,8(gam)\)