đốt cháy hoàn toàn m gam chất X cần dùng 4,48lít khí O2(đktc) thu đc 4,4g CO2 và3,6g H2O.Viết sơ đồ phản ứng và tính khối lượng X ban đầu đem đốt
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Sơ đồ X + O 2 → C O 2 + H 2 O ( 1 )
Áp dụng định luật bảo toàn khối lượng cho sơ đồ (1), ta có :
m + m O 2 = m C O 2 + m H 2 O
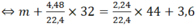
⇔ m = 1,6 gam

\(V_{CO_2}=0,5.22,4=11,2\left(l\right)\)
\(A_{CO_2}=0,5.6.10^{23}=3.10^{23}\) (phân tử \(CO_2\) )
2.
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
=> \(n_C=n_{CO_2}=0,1\left(mol\right)\) (1)
=> \(n_O=2nCO_2=0,1.2=0,2\left(mol\right)\) (*)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
=> \(n_H=2n_{H_2O}=0,2.2=0,4\left(mol\right)\) (2)
=> \(n_O=n_{H_2O}=0,2\left(mol\right)\) (**)
\(n_{O_2}=\dfrac{4,8}{22,4}=0,2\left(mol\right)\)
=> \(n_O=2n_{O_2}=2.0,2=0,4\left(mol\right)\) (3)
\(X+O_2\underrightarrow{t^o}CO_2+H_2O\)
Từ (1),(2),(3), (*), (**) suy ra: \(n_C:n_H:n_O=0,1:0,4:0\)
=> Công thức tổng quát của X là \(C_xH_y\)
có: \(x:y=n_C:n_H=0,1:0,4=1:4\)
=> X là: \(CH_4\)
Sơ đồ pứ: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(m_{CH_4}=3,6+0,2.44-0,2.32=6\left(g\right)\)

\(n_C=\dfrac{13,2}{44}=0,3\left(mol\right)\\ n_H=2.\dfrac{7,2}{18}=0,8\left(mol\right)\\ n_O=2.\dfrac{13,2}{44}+\dfrac{7,2}{18}-\dfrac{10,08}{22,4}=0,1\left(mol\right)\\ m_X=0,3.12+0,8+0,1.16=6\left(g\right)\\ CTPT:C_xH_yO_z\\ \Rightarrow x:y:z=0,3:0,8:0,1=3:8:1\)
Mà CTHH của X là CTDGN
=> CTHH của X: C3H8O
PTHHH: 2C3H8O + 9O2 ---to---> 6CO2 + 8H2O

\(a,Đặt:n_{CH_4}=a\left(mol\right);n_{C_4H_{10}}=b\left(mol\right)\left(a,b>0\right)\\ PTHH:CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ 2C_4H_{10}+13O_2\rightarrow\left(t^o\right)8CO_2+10H_2O\\ \Rightarrow\left\{{}\begin{matrix}16a+58b=7,4\\22,4a+22,4.4b=22\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}m_{CH_4}=0,1.16=1,6\left(g\right)\\m_{C_4H_{10}}=0,1.58=5,8\left(g\right)\end{matrix}\right.\\ b,n_{O_2}=2a+\dfrac{13}{2}b=2.0,1+6,5.0,1=0,85\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,85.22,4=19,04\left(l\right)\)

\(n_{O_2\left(đktc\right)}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ 4P+5O_2\underrightarrow{^{to}}2P_2O_5\\ 0,12........0,15.........0,06\left(mol\right)\\ m_P=0,12.31=3,72\left(g\right)\)

\(n_{C_2H_4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ PTHH:C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
0,25 0,5
\(\rightarrow m_{H_2O}=0,5.18=9\left(g\right)\)

a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)

