Trình bày cách pha 100ml dung dịch NaOH 0.05N biết MnaoH= 40g/mol
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Em hãy trình bày cách phe chế
100ml dung dịch HCL 0,25M bằng cách pha loãng dung dịch HCL 2,5M có sẵn

Ta có:
C1 = 2,5M (nồng độ dung dịch HCl ban đầu)
V1 = ? (thể tích dung dịch HCl ban đầu cần lấy)
C2 = 0,25M (nồng độ dung dịch HCl sau khi pha)
V2 = 100 ml (thể tích dung dịch sau khi pha)
Công thức pha loãng: C1 × V1 = C2 × V2
2,5 × V1 = 0,25 × 100
2,5 × V1 = 25
V1 = 25 / 2,5 = 10 ml
Vậy:
- Lấy 10 ml dung dịch HCl 2,5M
- Thêm nước cất vừa đủ để tổng thể tích là 100 ml
→ Ta thu được 100 ml dung dịch HCl 0,25M
Cho mình xin 1 tick với ạ
Để pha chế 100ml dung dịch HCl 0,25M từ dung dịch HCl 2,5M có sẵn, bạn cần thực hiện theo các bước sau.
1. Áp dụng công thức pha loãng
Bạn sử dụng công thức pha loãng dung dịch: C1⋅V1=C2⋅V2
Trong đó:
- C1: Nồng độ mol của dung dịch ban đầu (dung dịch HCl 2,5M).
- V1: Thể tích dung dịch ban đầu cần lấy (đang cần tìm).
- C2: Nồng độ mol của dung dịch cần pha (dung dịch HCl 0,25M).
- V2: Thể tích dung dịch cần pha (100ml).
2. Tính thể tích dung dịch HCl 2,5M cần lấy (V1)
Từ công thức trên, ta suy ra:
V1=C1C2⋅V2
Thay số vào, ta có:
V1=2,5M0,25M⋅100ml=10ml
Vậy, bạn cần lấy 10ml dung dịch HCl 2,5M.
3. Trình tự pha chế
- Dùng ống hút chia độ (pipet) lấy chính xác 10ml dung dịch HCl 2,5M cho vào bình định mức dung tích 100ml.
- Thêm từ từ nước cất vào bình định mức cho đến khi dung dịch gần đạt vạch 100ml.
- Dùng ống nhỏ giọt thêm từng giọt nước cất vào cho đến khi mực nước chạm đúng vạch 100ml của bình định mức.
- Đậy nút bình và lắc đều để dung dịch được đồng nhất.
Như vậy, bạn đã pha chế được 100ml dung dịch HCl 0,25M.

a)
m CuSO4 = 150.2% = 3(gam)
m dd CuSO4 20% = 3/20% = 15(gam)
m nước cần thêm = 150 - 15 = 135(gam)
Pha chế :
- Chuẩn bị 15 gam dd CuSO4 20% vào cốc
- Đong thêm 135 gam nước cho vào cốc, khuấy đều.
b) n NaOH = 0,25.9,5 = 2,375(mol)
V dd NaOH 2M = 1,1875(lít) = 1187,5(ml)
V nước cần bay hơi = 1187,5 - 250 = 937,5(ml)
- Chuẩn bị 1,1875 lít NaOH 2M vào cốc 2 lít có chia vạch
- Đun từ từ hỗn hợp cho nước bay hơi đến khi nước chạm vạch 250 ml thì dừng lại
\(a.\)
\(m_{CuSO_4}=150\cdot2\%=3\left(g\right)\)
\(m_{dd_{CuSO_4}}=\dfrac{3}{20\%}=15\left(g\right)\)
\(m_{H_2O\left(ct\right)}=150-15=135\left(g\right)\)
Chuẩn bị 15 gam dung dịch CuSO4 20% vào cốc 1 lít
Đong thêm 135 gam nước vào cốc,khuấy đều
\(b.\)
Anh sửa lại đề là : 0.5 M nhé !
\(n_{NaOH}=0.25\cdot0.5=0.125\left(mol\right)\)
\(V_{dd_{NaOH}}=\dfrac{0.125}{2}=0.0625\left(l\right)=62.5\left(ml\right)\)
\(V_{H_2O}=250-62.5=187.5\left(ml\right)\)
Chuẩn bị 62.5 ml dd NaOH 2M vào cốc 500 ml
Đong thêm 187.5 ml nước vào cốc,khuấy đều

a) Khối lượng chất tan cần để pha 150 g dung dịch CuSO4 2%: 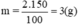
Khối lượng dung dịch CuSO4 20% ban đầu có chứa 3 g CuSO4: 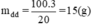
Khối lượng nước cần pha chế là: mnước = 150 – 15 = 135 g.
Pha chế: lấy 15 g dung dịch CuSO4 20% vào cốc thêm 135 g H2O vào và khuấy đều, được 150g dung dịch CuSO4 2%.
b) Số mol chất tan trong 250 ml dung dịch NaOH 0,5M.
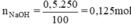
Thể tích dung dịch NaOH 2M có chứa 0,125 mol NaOH là:
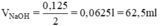
Pha chế: Đong lấy 62,5 ml dung dịch NaOH 2M cho vào cốc chia độ có dung tích 500ml. Thêm từ từ nước cất vào cốc đến vạch 250 ml và khuấy đều ta được 250 ml dung dịch 0,5M.

1)
m NaCl = 200.15% = 30(gam)
m H2O = 200 -30 = 170(gam)
- Pha chế : Cân lấy 30 gam NaCl cho vào cốc. Đong lấy 170 gam nước cho vào cốc khuấy đều
2) n Na2O = a(mol)
m NaOH = 400.15% = 40(gam)
Na2O + H2O → 2NaOH
a...............a............2a..........(mol)
Sau pư :
m dd = 400 + 62a - 18a = 400 + 44a(gam)
m NaOH = 2a.40 + 40 = 80a + 40(gam)
=> C% NaOH = (80a + 40) / (400 + 44a) .100% = 25%
=> a = 20/23
=> m Na2O = 62. 20/23 = 53,91 gam

a) n NaOH = 0,8.2 = 1,6 mol
m NaOH = 1,6.40 = 64 gam
Cân lấy 64 gam NaOH cho vào cốc có chia vạch
Thêm từ từ nước cho đến khi chạm vạch 800ml thì dừng lại,khuấy đều
b) m NaOH = 800.10% = 80(gam)
m H2O = 800 - 80 = 720 gam
Cân lấy 80 gam NaOH cho vào cốc có dung dịch 5 lít
Thêm 720 gam nước vào cốc, khuấy đều.
a) nNaOH= 2.0,8=1,6(mol)
PTHH: Na + H2O -> NaOH + 1/2 H2
=> nNa=1,6(mol)
=> Cho 800 ml nước vào 1,6 mol Na để tạo ra 800ml dung dịch NaOH 2M.
b) mNaOH= 800.10%=80(g)
=> nNaOH=80/40=2(mol)
PTHH: Na + H2O -> NaOH + 1/2 H2
=> nNa=2(mol) => mNa=2.23=46(g)
mH2= 1.2=2(g)
=> mH2O= mNaOH+ mH2- mNa= 800+ 2 - 2.23= 757g)
=> Điều chế: cho 756(g) nước vào 46 gam Na sẽ tạo ra 800 gam dd NaOH 10%.

1) Gọi thể tích các dung dịch NaOH có nồng độ 3% và 10% cần dùng lần lượt là V_1 và V_2.
m_NaOH 3%= 1,05(V_1)3%= 0,0315V_1.
m_NaOH 10% =1,12(V_2)10%= 0,112V_2.
m_NaOH 8%= 1,1.2000.8% =176.
Theo đề bài ta có hệ phương trình:
0,0315V_1 + 0,112V_2= 176 ∩ V_1+ V_2 =2000 => V_1= 96000/161 (mℓ), V_2= 226000/161 (mℓ).
- Tính toán:
Ta có: \(D=\dfrac{m_{dd_{NaOH}}}{0,5}=1,109\left(\dfrac{g}{ml}\right)\)
\(\Rightarrow m_{dd_{NaOH}}=0,5545\left(g\right)\)
Ta lại có: \(C_{\%_{NaOH}}=\dfrac{m_{NaOH}}{0,5545}.100\%=10\%\)
\(\Rightarrow m_{NaOH}=0,05545\left(g\right)\)
\(\Rightarrow m_{H_2O}=0,5545-0,05545=0,49905\left(g\right)\)
- Cách pha:
+ Chọn bình có thể tích trên 0,5 lít.
+ Cho 0,49905 gam nước vào bình.
+ Sau đó cho 0,05545 gam NaOH vào, khuấy đều là được dung dịch NaOH 10%.

a)
$m = D.V = 1,109.5.1000 =5545(gam)$
$m_{NaOH} = 5545.10\% = 554,5(gam)$
Pha :
- Cân lấy 554,5 gam NaOH khan cho vào cốc dung dịch 10 lít có chia vạch
- Thêm từ từ nước vào cho đến khi chạm vạch 5 lít, khuấy đều.
b)
$n_{NaOH} = \dfrac{545,5}{40} = 13,8625(mol)$
$C_{M_{NaOH}} = \dfrac{13,8625}{5} = 2,7725M$

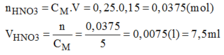
* Cách pha chế:
- Đong lấy 7,5ml dung dịch H N O 3 5M cho vào bình chứa.
- Cho thêm dần dần nước cất vào bình cho đến đủ 150ml lắc đều, ta được 150m dung dịch H N O 3 cần pha chế.