Cho 6,95 gam hỗn hợp gồm nhôm và sắt tác dụng với dung dịch H2SO4 loãng dư. Sau khi phản ứng xảy ra hoàn toàn thu được 3,92 l khí ở điểu kiện tiêu chuẩn.
a.Viết các phương trình hóa học
b. Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu.



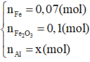
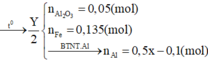
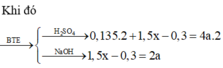
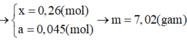
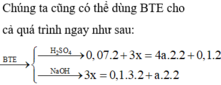
Đặt : \(n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m_{hh}=27a+56b=6.95\left(g\right)\left(1\right)\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(n_{H_2}=1.5a+b=\dfrac{3.92}{22.4}=0.175\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.05,b=0.1\)
\(\%Al=\dfrac{0.05\cdot27}{6.95}\cdot100\%=19.42\%\)
\(\%Fe=100-19.42=80.58\%\)
\(n_{H_2}=\dfrac{3,92}{22,4}=0,175(mol)\\ a,PTHH:2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ Fe+H_2SO_4\to FeSO_4+H_2\\b,n_{Al}=x(mol);n_{Fe}=y(mol)\\ \Rightarrow 27x+56y=6,95;1,5x+y=0,175\\ \Rightarrow x=0,05(mol);y=0,1(mol)\\ \Rightarrow \%_{Al}=\dfrac{0,05.27}{6,95}.100\%=19,42\%\\ \Rightarrow \%_{Fe}=100\%-19,42\%=80,58\% \)