Tính số mol của
c/ 12,8 gam SO2
d/ 3,36 lit H2 đktc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nFe = 11,2/56 = 0,2 (mol)
nKClO3 = 24,5/122,5 = 0,2 (mol)
nCaCO3 = 40/100 = 0,4 (mol)
nH2 = 8,96/22,4 = 0,4 (mol)
nCO2 = 5,6/22,4 = 0,25 (mol)
nSO2 = 3,36/22,4 = 0,15 (mol)
a)11,2g fe
n Fe=\(\dfrac{11,2}{56}\) =0,5 mol
24,5g KCIO3
=>n KClO3=\(\dfrac{24,5}{122,5}\)=0,2 mol
40g CaCO3
=>n CaCO3=\(\dfrac{40}{100}\)=0,4 mol
b)8,96 lit H2
=>n H2=\(\dfrac{8,96}{22,4}\) =0,4 mol
5,6 lit Co2
=>n CO2=\(\dfrac{5,6}{22,4}\) =0,25 mol
3,36 lit So2
=>n SO2=\(\dfrac{3,36}{22,4}\)=0,15 mol

\(n_{Co_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_{N_2}=\dfrac{44,8}{22,4}=2mol\)

Gọi số mol của Ba, Al và Mg lần lượt là x, y và z mol
Lượng khí thu được khi cho A vào nước dư ít hơn khi cho A vào xút dư nên khi cho A vào nước dư thì Ba phản ứng hết, Al phản ứng một phần. Khi cho A vào xút dư thì cả Ba và Al đều phản ứng hết.
Cho A tác dụng với nước dư có phản ứng:
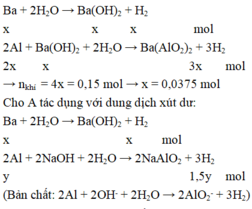

Khối lượng của A là: m = 0,0375.137 + 0,175.27 + 0,1.24 = 12,2625 gam.
⇒ Chọn B

\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
0,15<--------------------0,15
=> \(\%Fe=\dfrac{0,15.56}{14,8}.100\%=56,757\%\)
=> \(\%Cu=100\%-56,757\%=43,243\%\)
nH2 = 3,36/22,4 = 0,15 (mol)
PTHH: Fe + 2HCl -> FeCl2 + H2
nFe = 0,15 (mol)
mFe = 0,15 . 56 = 8,4 (g)
%mFe = 8,4/14,8 = 56,75%
%mCu = 100% - 56,75% = 43,25%

\(4.\)
\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.15.....0.3....................0.15\)
\(m_{Fe}=0.15\cdot56=8.4\left(g\right)\)
\(C_{M_{HCl}}=\dfrac{0.3}{0.5}=0.6\left(M\right)\)
\(5.\)
\(Đặt:n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(m_{hh}=56a+27b=8.3\left(g\right)\left(1\right)\)
\(n_{H_2}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Rightarrow a+1.5b=0.25\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%Fe=\dfrac{5.6}{8.3}\cdot100\%=67.47\%\)
\(\%Al=32.53\%\)
bạn ơi cho mik hỏi: tại sao lại suy ra: a+1,5b=0,25 vậy ạ ? và cả bước tiếp theo nx ạ ?

c)
\(n_{H_2}=\dfrac{m}{M}=\dfrac{13,2}{2}=6,6\left(mol\right)\)
d)
\(n_{SO_2}=\dfrac{m}{M}=\dfrac{12,8}{32+16\cdot2}=0,2\left(mol\right)\)
đề cho khối lượng thì tính số mol của các chất khí ơ dktc là sao vậy bn?=))

\(a.V_{N_2}=n.22,4=0,25.22,4=5,6\left(l\right)\)
\(b.n_{NH_3}=\dfrac{0,9.10^{23}}{6.10^{23}}=0,15\left(mol\right)\\ V_{NH_3}=n.22,4=0,15.22,4=3,36\left(l\right)\)
\(c.n_{SO_2}=\dfrac{3,2}{64}=0,05\left(mol\right)\\ V_{SO_2}=n.22,4=0,05.22,4=1,12\left(l\right)\)
\(n_{SO_2}=\dfrac{12.8}{64}=0.2\left(mol\right)\)
\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)