Đốt cháy hoàn toàn 0,1 mol hiđrocacbon, rồi cho toàn bộ sản phẩm cháy hấp thụ vào bình đựng lượng dư dung dịch NaOH thấy khối lượng của bình tăng lên 23 gam. Xác định công thức phân tử của hiđrocacbon và cho biết số công thức cấu tạo thu gọn dạng mạch hở có thể có, biết là chất khí C≤4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


n X = 4,48/22,4 = 0,2 mol
=> n CH 4 = 0,2/4 = 0,05 mol; n A = 0,05 x 3 = 0,15 mol
Phương trình hóa học: CH 4 + 2 O 2 → C O 2 + 2 H 2 O
C n H m + (n+m/4) O 2 → t ° nC O 2 + m/2 H 2 O
C H 2 + Ca OH 2 → CaC O 3 + H 2 O
n CO 2 = n CaCO 3 = 50/100 = 0,5 mol => n CO 2 , n H 2 O tạo ra khi đốt cháy A là
n CO 2 = 0,5 - 0,05 = 0,45mol; n H 2 O = 0,7 - 0,1 = 0,6 mol
=> Công thức của A là C 3 H 8

Đáp án D
Đặt
![]()
12a+2b =4,872
44a+18b=27,935,586
=>a=0,336; b=0,42
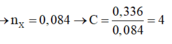

Đáp án B
Ta có nCO2 = 0,3 mol ⇒ CTrung bình = 0,3/0,2 = 1,5.
⇒ Hỗn hợp ban đầu chứa CH4 và đồng đẳng của nó.
⇒ nH2O = nCO2 + nAnkan = 0,5 mol.
Mà mBình tăng = mCO2 + mH2O = 0,3×44 + 0,5×18 = 22,2 gam

Đáp án B
Ta có nCO2 = 0,3 mol ⇒ CTrung bình = 0 , 3 0 , 2 = 1,5.
⇒ Hỗn hợp ban đầu chứa CH4 và đồng đẳng của nó.
⇒ nH2O = nCO2 + nAnkan = 0,5 mol.
Mà mBình tăng = mCO2 + mH2O = 0,3×44 + 0,5×18 = 22,2 gam.

Đáp án D
Ta có mCO2 + mH2O + mdd Ba(OH)2 = mkết tủa + mddsau phản ứng
mCO2 + mH2O = mkết tủa + mddsau phản ứng – mdd Ba(OH)2= 39,4 – 19,912 = 19,488g
Gọi x = nCO2, y = nH2O
44x + 18y = 19,488 và 12x + 2y = 4,64
x = 0,348 và y = 0,232
nCO2 : nH2O = 0,348 : 0,232
Hay nC : nH = 0,348 : 0,464 = 3 : 4 Hiđrocacbon là C3H4
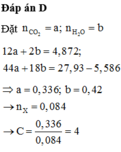


CTPT hiđrocacbon là CxHy ( x, y ∈ N và 0< y ≤ 2x + 2)
CxHy + (x +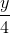 ) O2 → x CO2 +
) O2 → x CO2 + 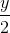 H2O
H2O
0,1 mol → 0,1x→ 0,05y
=> Khối lượng CO2 + Khối lượng H2O = 0,1.x . 44 + 0,05y. 18 =23
=> y =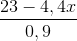
=> 0 <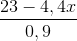 ≤ 2x + 2
≤ 2x + 2
=> 3,3 < x < 5,2 => x = 4 hoặc x =5
Nếu x = 4 => y =6 => CTPT là C4H6. Nếu x =5 => y = 1,1 ( Loại)
Vậy công thức phân tử của hiđrocacbon thỏa mãn là C4H6.
Công thức cấu tạo mạch hở có thể có:
CH2 = CH – CH = CH2
CH2 = C= CH – CH3
CH ≡ C – CH2 – CH3
CH3 – C ≡ C – CH3
sao ra đc 3,3 và 5,2 ở chỗ 3,3 < x < 5,2