Đốt cháy hoàn toàn 1,72 gam chất hữu cơ (E) thu được 3,52 gam CO2; 1,80 gam H2O và một lượng khí N2. Tìm công thức phân tử của E. biết khi hoá hơi 1,29 gam E thì thu được thể tích hơi đúng bằng thể tích 0,96 gam oxi trong cùng điều kiện
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{CO_2}=\dfrac{4.62}{44}=0.105\left(mol\right)\Rightarrow n_C=0.105\left(mol\right)\Rightarrow m_C=1.26\left(g\right)\)
\(n_{H_2O}=\dfrac{1.215}{18}=0.0675\left(mol\right)\Rightarrow n_H=0.135\left(mol\right)\)
\(n_{N_2}=\dfrac{0.168}{22.4}=0.0075\left(mol\right)\Rightarrow n_N=0.015\left(mol\right)\Rightarrow m_N=0.015\cdot14=0.21\left(g\right)\)
\(m_O=1.605-1.26-0.135-0.21=0\)
\(Gọi:CTHH:C_xH_yN_z\)
\(x:y:z=0.105:0.135:0.015=7:9:1\)
\(CT:C_7H_9N\)

Câu 7:
\(n_{CO_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\)
Bảo toàn C: nC = 0,6 (mol)
Bảo toàn H: nH = 1,2 (mol)
=> \(n_O=\dfrac{10,8-0,6.12-1,2}{16}=0,15\left(mol\right)\)
=> nC : nH : nO = 0,6 : 1,2 : 0,15 = 4:8:1
=> CTPT: (C4H8O)n
Mà M = 2,25.32 = 72(g/mol)
=> n = 1
=> CTPT: C4H8O
Câu 6
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
Bảo toàn C: nC = 0,25 (mol)
Bảo toàn H: nH = 0,6 (mol)
=> \(n_O=\dfrac{4,4-0,25.12-0,6.1}{16}=0,05\left(mol\right)\)
nC : nH : nO = 0,25 : 0,6 : 0,05 = 5:12:1
=> CTPT: (C5H12O)n
Mà M = 44.2=88(g/mol)
=> n = 1
=> CTPT: C5H12O
Câu 8:
MX = 1,875.32 = 60 (g/mol)
Giả sử có 1 mol chất X => mX = 60.1 = 60 (g)
\(m_C=\dfrac{60.40}{100}=24\left(g\right)=>n_C=\dfrac{24}{12}=2\left(mol\right)\)
\(m_H=\dfrac{60.6,67}{100}=4\left(g\right)=>n_H=\dfrac{4}{1}=4\left(mol\right)\)
\(m_O=60-24-4=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> Trong 1 mol X chứa 2 mol C, 4 mol H, 2 mol O
=> CTPT: C2H4O2

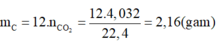
Dựa vào 4 đáp án, ta thấy chỉ có nguyên tố C và H ![]()
Gọi công thức phân tử cần tìm là CxHy.
Ta có: 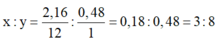 . Do đó CTPT của A có dạng (C3H8)n
. Do đó CTPT của A có dạng (C3H8)n
Ta áp dụng điều kiện: ![]()
Mà n là số nguyên nên n = 1. Vậy công thức phân tử của chất A là C3H8.
Đáp án C.

Đáp án B
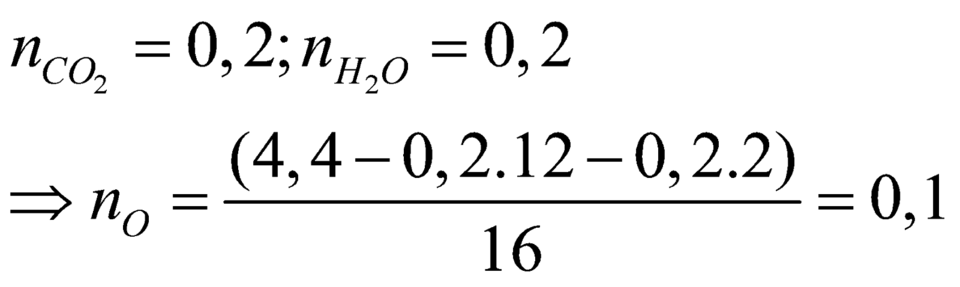
X tác dụng với NaOH sinh muối thì X là este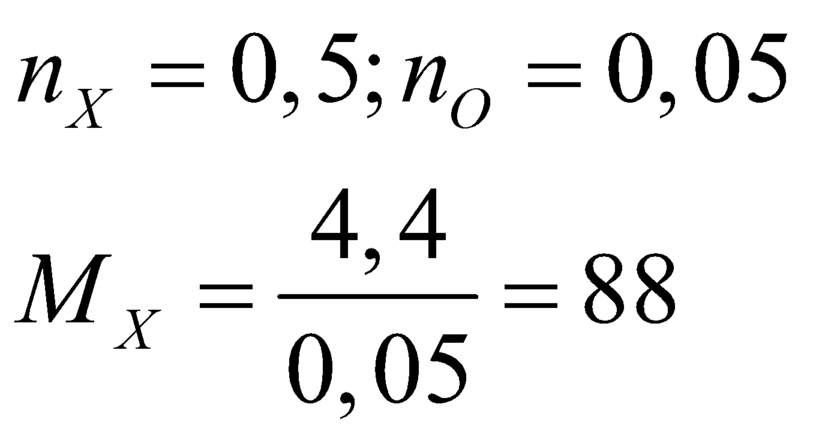
M có CTPT là ![]()
![]()
![]()
metyl propionat.

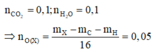
=> Công thức đơn giản nhất của X là C2H4O
=> Công thức phân tử của X là C2nH4nOn
Do đó ta loại được đáp án A và D. Đáp án B và C đều có công thức phân tử là C4H8O2.
Mà rnmuối > mX => gốc ancol -R có MR < MNa = 23
=> X là C2H5COOCH3
Đáp án C

Chọn đáp án C
nCO2 = 0,4 mol < nH2O = 0,6 mol ⇒ Y là ancol no, mạch hở.
và nY = nH2O – nCO2 = 0,6 – 0,4 = 0,2 mol ⇒ CY 0,4 ÷ 0,2 = 2.
Lại có 20,3 gam chất hữu cơ có CTPT là C9H17O4N ⇔ 0,1 mol = ½nancol Y
⇒ Y là ancol đơn chức và hợp chất hữu cơ chứa 2 nhóm chức este.!
ancol C2 Y là C2H5OH → cấu tạo hợp chất hữu cơ là H2NC3H5(COOC2H5)2.
⇒ muối X là H2NC3H5(COONa)2 ⇔ CTPT C5H7O4NNa2.
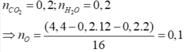
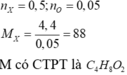
\(n_{CO_2}=\dfrac{3.52}{44}=0.08\left(mol\right)\)
\(n_{H_2O}=\dfrac{1.8}{18}=0.1\left(mol\right)\)
\(m_N=1.72-0.08\cdot12-0.1\cdot2=0.56\left(g\right)\)
\(n_N=\dfrac{0.56}{14}=0.04\left(mol\right)\)
\(M_E=\dfrac{1.29}{\dfrac{0.96}{32}}=43\left(đvc\right)\)
\(n_E=\dfrac{1.72}{43}=0.04\left(mol\right)\)
Số nguyên tử C : \(\dfrac{0.08}{0.04}=2\)
Số nguyên tử H : \(\dfrac{0.2}{0.04}=5\)
Số nguyên tử N : \(\dfrac{0.04}{0.04}=1\)
\(CT:C_2H_5N\)