Hỗn hợp khí X gồm 2 hiđrocacbon A và B là đồng đẳng kế tiếp. Đốt cháy X với 64 gam \(O_2\) (dư) rồi dẫn sản phẩm thu được qua bình đựng \(Ca\left(OH\right)_2\) dư thu được 100 g kết tủa. Khí ra khỏi bình có thể tích 11,2 lít ở \(0^oC\) và 0,4 atm. Xác định công thức phân tử của A và B.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Từ giả thiết suy ra :
n C O 2 = n C a C O 3 = 100 100 = 1 m o l ; n O 2 p ư = n O 2 b đ - n O 2 d ư = 64 32 - 11 , 2 . 0 , 4 0 , 082 . 273 = 1 , 8 m o l .
Đặt công thức phân tử trung bình của A và B là C n ¯ H 2 n ¯ + 2
Phương trình phản ứng cháy:
C n ¯ H 2 n ¯ + 2 + 3 n ¯ + 1 2 O 2 → n ¯ C O 2 + ( n ¯ + 1 ) H 2 O ( 1 ) m o l x → 3 n ¯ + 1 2 . x → n ¯ . x
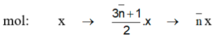


Ta có: \(n_{O_2\left(banđau\right)}=\dfrac{62}{32}=2\left(mol\right)\)
\(n_{CO_2}=n_{CaCO_3}=\dfrac{100}{100}=1\left(mol\right)\)
Khí thoát ra khỏi bình là O2 dư.
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{pV}{RT}=\dfrac{0,4.11,2}{0,082.273}=0,2\left(mol\right)\)
\(\Rightarrow n_{O_2\left(pư\right)}=2-0,2=1,8\left(mol\right)\)
BTNT O, có: \(2n_{O_2\left(pư\right)}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=2.1,8-2.1=1,6\left(mol\right)\)
Vì đốt cháy 2 hiđrocacbon thu được nH2O > nCO2 nên A và B là ankan.
⇒ nankan = 1,6 - 1 = 0,6 (mol)
Gọi CTPT chung của A và B là \(C_{\overline{n}}H_{2\overline{n}+2}\)
\(\Rightarrow\overline{n}=\dfrac{1}{0,6}=1,667\)
Vậy: A và B là CH4 và C2H6.
Bạn tham khảo nhé!

a)
\(n_{BaCO_3}=\dfrac{78,8}{197}=0,4\left(mol\right)\)
=> \(n_{CO_2}=0,4\left(mol\right)\)
=> \(n_{H_2O}=\dfrac{22,1-0,4.44}{18}=0,25\left(mol\right)\)
Do \(n_{CO_2}>n_{H_2O}\)
=> 2 hidrocacbon thuộc dãy đồng đẳng ankin hoặc ankadien
Bảo toàn C: nC = 0,4 (mol)
Do \(\overline{C}=\dfrac{0,4}{0,15}=2,67< 3\)
=> 2 hidrocacbon thuộc dãy đồng đẳng ankin
b)
Do \(\overline{C}=2,67\)
=> Trong X có C2H2 (etin)
Giả sử A là C2H2
Gọi CTPT của B là CnH2n-2
TH1: \(\left\{{}\begin{matrix}n_A+n_B=0,15\\n_A:n_B=1:2\end{matrix}\right.\)
=> nA = 0,05 (mol); nB = 0,1 (mol)
Bảo toàn C: 2.0,05 + 0,1.n = 0,4
=> n = 3
=> B là C3H4 (propin)
TH2: \(\left\{{}\begin{matrix}n_A+n_B=0,15\\n_B:n_A=1:2\end{matrix}\right.\)
=> nA = 0,1 (mol); nB = 0,05 (mol)
Bảo toàn C: 0,1.2 + 0,05.n = 0,4
=> n = 4
=> B là C4H6
C4H6 có 2 đồng phân ankin
+ \(CH\equiv C-CH_2-CH_3\) (but-1-in)
+ \(CH_3-C\equiv C-CH_3\) (but-2-in)

Đáp án C
m gam hhX gồm 2 ancol kế tiếp + O2 → CO2 + H2O
Dẫn sản phẩm + Ca(OH)2 dư
→ mbình tăng = 19,1 gam và 0,25 mol ↓CaCO3.
Oxi hóa m gam X bằng CuO, lấy sản phẩm + AgNO3/NH3 → x gam Ag.
• nCO2 = 0,25 mol
→ nH2O = (19,1 - 0,25 x 44) : 18 = 0,45 mol
→ Ancol no, đơn chức.
nhhX = 0,45 - 0,25 = 0,2 mol
→ số C trung bình = 0,25 : 0,2 = 1,25
→ CH3OH và C2H5OH.
Đặt nCH3OH = x mol; nC2H5OH = y mol.
Ta có hpt:
![]()
nAg = 4 x nHCHO + 2 x nCH3CHO
= 4 x 0,15 + 2 x 0,05 = 0,7 mol.
⇒ x = 0,7 x 108 = 75,6 gam

Đáp án C
m gam hhX gồm 2 ancol kế tiếp + O2 → CO2 + H2O
Dẫn sản phẩm + Ca(OH)2 dư → mbình tăng = 19,1 gam và 0,25 mol ↓CaCO3.
Oxi hóa m gam X bằng CuO, lấy sản phẩm + AgNO3/NH3 → x gam Ag.
• nCO2 = 0,25 mol → nH2O = (19,1 - 0,25 x 44) : 18 = 0,45 mol → Ancol no, đơn chức.
nhhX = 0,45 - 0,25 = 0,2 mol → số C trung bình = 0,25 : 0,2 = 1,25 → CH3OH và C2H5OH.
Đặt nCH3OH = x mol; nC2H5OH = y mol.
nAg = 4 x nHCHO + 2 x nCH3CHO = 4 x 0,15 + 2 x 0,05 = 0,7 mol.
⇒ x = 0,7 x 108 = 75,6 gam

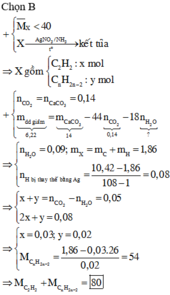

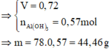

Vì A và B là hiđrocacbon nên khi đốt cháy chỉ thu được CO2 và H2O.
Ta có: \(n_{O_2}=\dfrac{64}{32}=2\left(mol\right)\)
\(n_{CO_2}=n_{CaCO_3}=\dfrac{100}{100}=1\left(mol\right)\)
Khí ra khỏi bình là O2 dư.
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{pV}{RT}=\dfrac{0,4.11,2}{0,082.273}=0,2\left(mol\right)\)
BTNT O, có: \(n_{H_2O}=2n_{O_2}-2n_{O_2\left(dư\right)}-2n_{CO_2}=1,6\left(mol\right)\)
Có: nH2O > nCO2 nên A và b là ankan.
⇒ nankan = nH2O - nCO2 = 0,6 (mol)
Giả sử CTPT chung của A và B là: \(C_{\overline{n}}H_{2\overline{n}+2}\).
Có: n = số nguyên tử C = \(\dfrac{1}{0,6}=1,67\)
Mà: A và B là 2 ankan kế tiếp.
Nên A và B lần lượt là CH4 và C2H6.
Bạn tham khảo nhé!