cho m gam (mg+al2o3) tác dụng vừa đủ với 400ml đ HCL 2( khối lượng riêng là 1.2gam/ml) thu được dung dịch X và 2.24dm^3 khí sinh ra ở đktc. tính m và nồng độ % các chất tan trong dung dịch x
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nH2 = 0,03 ⇒ nAl = 0,02 ⇒ mAl = 0,54g
⇒ mAl2O3 = ⇒ nAl2O3 bđ = 0,03
Bảo toàn nguyên tố Al ⇒ nNaAlO2 = nAl + 2nAl2O3 bđ = 0,08
nAl2O3 thu được = 3,57/102 = 0,035 ⇒ nAl(OH)3 = 0,07
Trường hợp 1: NaAlO2 + HCl + H2O → Al(OH)3 + NaCl
⇒ HCl = nAl(OH)3 = 0,07 [HCl] = 0,07/0,2 = 0,35M
Trường hợp 2:
NaAlO2 + HCl + H2O → Al(OH)3 + NaCl
0,07 ← 0,07 ← 0,07
NaAlO2 + 4HCl → AlCl3 + NaCl + 2H2O
(0,08 – 0,07) → 0,04
⇒ nHCl = 0,11 ⇒ [HCl] = 0,11/0,2 = 0,55M
Vậy chọn D.

a) CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
b) \(n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\)
CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
_0,1---->0,2------->0,1----->0,1
=> mCaCl2 = 0,1.111 = 11,1 (g)
=> VCO2 = 0,1.22,4 = 2,24 (l)
c) \(a=C_{M\left(HCl\right)}=\dfrac{0,2}{0,4}=0,5M\)
d) \(C_{M\left(CaCl_2\right)}=\dfrac{0,1}{0,4}=0,25M\)

a) 2Al + 6HCl -> 2AlCl3 + 3H2
Al2O3 + 6HCl -> 2AlCl3 + 3H2O
nH2 = 0,15mol => nAl=0,1mol => mAl=2,7g; mAl2O3 = 10,2g => nAl2O3 = 0,1mol
=>%mAl=20,93% =>%mAl2O3 = 79,07%
b) nHCl = 0,1.3+0,1.6=0,9 mol=>mHCl(dd)=100g
mddY=12,9+100-0,15.2=112,6g
mAlCl3=22,5g=>C%=19,98%

n A l : n A l 2 O 3 = 2 : 3 n A l = 2 n H 2 3 = 0 , 02 ⇒ n A l 2 o 3 = 0 , 03
Sơ đồ: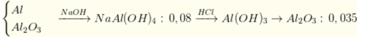
⇒ n H C l = 0 , 07 + ( 0 , 08 - 0 , 07 ) . 4 = 0 , 11 ⇒ [ H C l ] = 0 , 11 0 , 2 = 0 , 55
Đáp án C





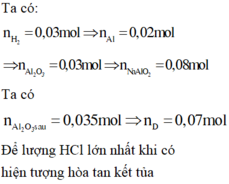
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
Ta có: \(\left\{{}\begin{matrix}\Sigma n_{HCl}=0,4\cdot2=0,8\left(mol\right)\\n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,1mol\\n_{Al_2O_3}=0,1mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Al_2O_3}=0,1\cdot102=10,2\left(g\right)\\m_{Mg}=0,1\cdot24=2,4\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{hh}=10,2+2,4=12,6\left(g\right)\)
Theo PTHH: \(\left\{{}\begin{matrix}n_{MgCl_2}=n_{Mg}=0,1mol\\n_{AlCl_3}=2n_{Al_2O_3}=0,2mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{MgCl_2}=0,1\cdot95=9,5\left(g\right)\\m_{AlCl_3}=0,2\cdot133,5=26,7\left(g\right)\end{matrix}\right.\)
Mặt khác: \(\left\{{}\begin{matrix}m_{ddHCl}=400\cdot1,2=480\left(g\right)\\m_{H_2}=0,1\cdot2=0,2\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{dd}=m_{hh}+m_{ddHCl}-m_{H_2}=492,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{9,5}{492,4}\cdot100\%\approx1,93\%\\C\%_{AlCl_3}=\dfrac{26,7}{492,4}\cdot100\%\approx5,42\%\end{matrix}\right.\)