Để 13g bột kẽm tác và 8,1g bột nhôm trong không khí một thời gian , thu được 27,5g chất rắn B. Cho B tác dụng với dung dịch HCl dư thu được bao nhiêu lít khí(đktc) ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1)
- Trong A chứa Al, Cu, Ag
- Do trong A chứa Cu => Ag bị đẩy ra hết khỏi dd
- Do cho B tác dụng với NaOH dư thu được kết tủa
=> Trong B chứa Al(NO3)3, Cu(NO3)2
Al + 3AgNO3 --> Al(NO3)3 + 3Ag
2Al + 3Cu(NO3)2 --> 2Al(NO3)3 + 3Cu
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
Al(NO3)3 + 3NaOH --> Al(OH)3 + 3NaNO3
Al(OH)3 + NaOH --> NaAlO2 + 2H2O
Cu(NO3)2 + 2NaOH --> Cu(OH)2 + 2NaNO3
Cu(OH)2 --to--> CuO + H2O
2)
Rắn sau khi nung là CuO
\(n_{CuO}=\dfrac{1,6}{80}=0,02\left(mol\right)\)
=> \(n_{Cu\left(NO_3\right)_2\left(B\right)}=0,02\left(mol\right)\)
\(n_{H_2}=\dfrac{0,1008}{22,4}=0,0045\left(mol\right)\)
PTHH: 2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,003<---------------------------------0,0045
Bảo toàn Al: \(n_{Al\left(NO_3\right)_3\left(B\right)}=\dfrac{0,81}{27}-0,003=0,027\left(mol\right)\)
Gọi số mol Cu, Ag trong hỗn hợp kim loại là a, b (mol)
=> 64a + 108b = 6,012 (1)
Bảo toàn Ag: \(n_{AgNO_3\left(X\right)}=b\left(mol\right)\)
Bảo toàn Cu: \(n_{Cu\left(NO_3\right)_2\left(X\right)}=a+0,02\left(mol\right)\)
Bảo toàn \(NO_3^-\): \(n_{AgNO_3\left(X\right)}+2.n_{Cu\left(NO_3\right)_2\left(X\right)}=3.n_{Al\left(NO_3\right)_3\left(B\right)}+2.n_{Cu\left(NO_3\right)_2\left(B\right)}\)
=> \(b+2a+0,04=3.0,027+2.0,02\)
=> 2a + b = 0,081 (2)
(1)(2) => a = 0,018 (mol); b = 0,045 (mol)
=> \(\left\{{}\begin{matrix}n_{AgNO_3\left(X\right)}=0,045\left(mol\right)\\n_{Cu\left(NO_3\right)_2\left(X\right)}=0,038\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(AgNO_3\right)}=\dfrac{0,045}{0,2}=0,225M\\C_{M\left(Cu\left(NO_3\right)_2\right)}=\dfrac{0,038}{0,2}=0,19M\end{matrix}\right.\)

Đáp án A
Ta có sơ đồ phản ứng:
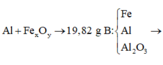
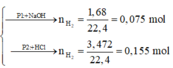
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
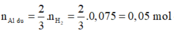
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
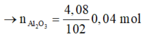
Ta có:
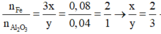
=> Oxit sắt cần tìm là Fe2O3

Chất rắn ko tan là Cu
Đặt \(n_{Mg}=x(mol);n_{Al}=y(mol)\Rightarrow 24x+27y=13-4=9(1)\)
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45(mol)\\ PTHH:Mg+2HCl\to MgCl_2+H_2\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow x+1,5y=0,45(2)\\ (1)(2)\Rightarrow x=0,15(mol);y=0,2(mol)\\ a,\%_{Cu}=\dfrac{4}{13}.100\%=30,77\%\\ \%_{Mg}=\dfrac{0,15.24}{13}.100\%=27,69\%\\ \%_{Al}=100\%-30,77\%-27,69\%=41,54\%\\ b,\Sigma n_{HCl}=2x+3y=0,9(mol)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,9}{2}=0,45(l)\)





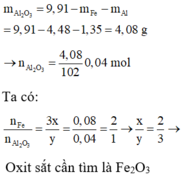



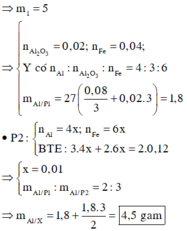

\(n_{Zn} = \dfrac{13}{65} = 0,2(mol) ; n_{Al} = \dfrac{8,1}{27} = 0,3(mol)\)
Bảo toàn khối lượng :
\(m_{O_2} = 27,5 - 13 - 8,1 = 6,4(gam)\\ \Rightarrow n_{O_2} = \dfrac{6,4}{32}=0,2(mol)\)
Bảo toàn e :
\(2n_{Zn} + 3n_{Al} = 4n_{O_2} + 2n_{H_2}\\ \Rightarrow n_{H_2} = \dfrac{0,2.2 + 0,3.3-0,2.4}{2}=0,25(mol)\\ \Rightarrow V_{H_2} = 0,25.22,4 = 5,6(lít)\)