cho 24.8 gam n2o tác dụng với dung dịch chứa 50.4 gam hno3.tính khối lượng các chất thu được sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(n_{Na_2O}=\dfrac{24,8}{62}=0,4\left(mol\right)\)
\(n_{HNO_3}=\dfrac{50,4}{63}=0,8\left(mol\right)\)
PT: \(Na_2O+2HNO_3\rightarrow2NaNO_3+H_2O\)
____0,4_____0,8_________0,8 (mol)
→ Pư vừa đủ.
\(\Rightarrow m_{NaNO_3}=0,8.85=68\left(g\right)\)
Bạn tham khảo nhé!

PTK trung bình của hỗn hợp NO và N2O = 18,5 x 2 = 37
--> n NO = n N2O = 4,48/44,8 = 0,1 mol
--> n HNO3 = 1,1(0,1 x 4 + 0,1 x 10) = 1,54 mol
--> Cm HNO3 = 1,54/2 = 0,77 lít = 770 ml.
m muối = 13,4 + 0,1 x 3 x 62 + 0,1 x 8 x 62 = 81,6 gam.

Chọn đáp án C
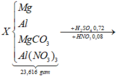
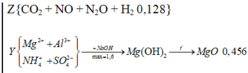
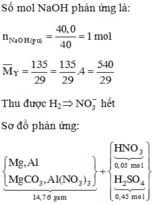
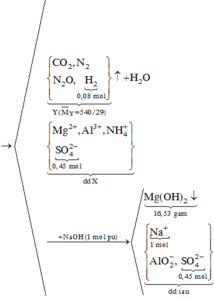
nMgO = 18,24/40 = 0,456 và n S O 4 2 - trong Y = 0,72 => nAl3+ trong Y =1,6 − 0,72×2 = 0,16
BTÐT => n N H 4 + = 0,72x2 − 0,16×3 − 0,456×2 = 0,048
Dễ thấy đề không cho quá nhiều dữ kiện về hỗn hợp khí Z, nhưng lại cho nH2 và bắt tìm phần trăm khối lượng H2 => Chỉ cần tìm khối lượng của Z, không cần tìm cụ thể số mol
Nhận thấy có đủ số mol ở tất cả các chất chứa hiđro trong quá trình
nH2O sau khi X tác dụng với axit = 0,72 + 0,08/2 – 0,128 – 0,048x2= 0,536
BTKL=>23,616+0,72×98+0,08×63 = mZ+0,456×24+0,16×27+0,048×18+0,72×96+0,536×18
=> mZ = 4,32 gam

Đáp án B

BTNT: N => nHNO3 = nNH4+ + 2nN2O + nNO = t + 0,094 (mol)
BTNT: H => nHNO3 + nHCl = 4nNH4+ + 2nH2O
=> nH2O = [(t + 0,094) + 1,726 – 4t]/2 = 0,91 – 1,5t
BTNT: O => 4z + 3( t + 0,094) = 0,062 + ( 0,91 – 1,5t) (1)
BTĐT đối với các chất trong dd Y
=> 2x+ 2y + 0,06.2 + 3. (3z- 0,06) + t = 1,726 (2)
mmuối = 24x + 65y + 56.3z + 18t + 1,726.35,5 = 95,105 (3)
m↓ = 58y + 0,06.90 + 107( 3z- 0,06) = 54,554
=> 58y +321z = 55, 574 (4)
Giải hệ (1), (2), (3) và (4) => x = 0,128 ; y = 0,08 ; z = 0,15 ; t = 0,02 (mol)
=> m = 0,128. 24 + 0,08.65 + 0,15. 232 = 43,072 (g)
Gần nhất với 43 gam

n H2SO4=\(\dfrac{10\%.490}{2+32+16.4}=0,5mol\)
n Al2O3 =\(\dfrac{10,2}{27.2+16.3}=0,1mol\)
\(Al_2O_3+3H_2SO_4->Al_2\left(SO_4\right)_3+3H_2O\)
bđ 0,1............0,5
pư 0,1............0,3..................0,1
spu 0 ................0,2................0,1
=> sau pư gồm H2SO4 dư , Al2(S04)3 và H2O
m H2SO4 dư = \(0,2.\left(2+32+16.3\right)=19,6g\)
m Al2(SO4)3 = \(0,1\left(27.2+32.3+16.4.3\right)=34,2g\)
m dd = \(490+10,2=500,2g\)
% Al2(SO4)3 = \(\dfrac{34,2}{500,2}.100\sim6,84\%\)
% H2SO4 dư = \(\dfrac{19,6}{500,2}.100\sim3,92\%\)

\(n_{Fe_2O_3}=\dfrac{3.2}{160}=0.02\left(mol\right)\)
\(n_{HCl}=\dfrac{2.19}{36.5}=0.06\left(mol\right)\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(1...........6\)
\(0.02...........0.06\)
Lập tỉ lệ : \(\dfrac{0.02}{1}>\dfrac{0.06}{6}\Rightarrow Fe_2O_3dư\)
\(n_{Fe_2O_3\left(dư\right)}=0.02-\dfrac{0.06}{6}=0.01\left(mol\right)\)
\(m_{Fe_2O_3\left(dư\right)}=0.01\cdot160=1.6\left(g\right)\)
\(m_{FeCl_3}=0.02\cdot162.5=3.25\left(g\right)\)
\(m_{H_2O}=0.03\cdot18=0.54\left(g\right)\)
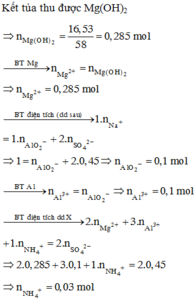
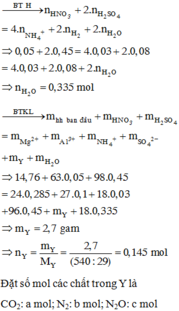


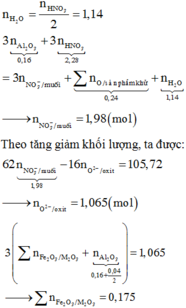


Sửa đề : 24.8 (g) Na2O
\(n_{Na_2O}=\dfrac{24.8}{62}=0.4\left(mol\right)\)
\(n_{HNO_3\left(dư\right)}=\dfrac{50.4}{63}=0.8\left(mol\right)\)
\(Na_2O+2HNO_3\rightarrow2NaNO_3+H_2O\)
\(0.4............0.8..............0.8...........0.4\)
\(m_{NaNO_3}=0.8\cdot85=68\left(g\right)\)
\(m_{H_2O}=0.4\cdot18=7.2\left(g\right)\)