Đun nóng 14,3 gam hỗn hợp X gồm Al, Zn, Mg trong không khí thu được a gam hỗn hợp Y gồm các kim loại và các oxit. Hoà tan hoàn toàn lượng hỗn hợp Y trên trong dung dịch HCl dư thu được 4,48 lít khí H2 (đktc) và dung dịch Z. Cô cạn Z được 49,8 gam muối khan. Xác định giá trị của a.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có sơ đồ chuyển hoá :
Mg, Zn, Al → O 2 MgO, ZnO, Al 2 O 3
MgO + 2HCl → MgCl 2 + H 2 O
ZnO + 2HCl → ZnCl 2 + H 2 O
Al 2 O 3 + 6HCl → 2 AlCl 3 + 3 H 2 O
MgO, ZnO, Al 2 O 3 → HCl MgCl 2 , ZnCl 2 , AlCl 3
Ta có khối lượng O 2 đã phản ứng : m O 2 = 20,3 - 13,1 = 7,2 (g)
Vậy khối lượng oxi trong hỗn hợp oxit là 7,2 gam.
Toàn bộ lượng oxi trong oxit đã chuyển vào H 2 O nên ta có m O ( H 2 O ) = 7,2g
Cứ 1 mol H 2 O thì chứa 1 mol nguyên tử O ⇒ n H 2 O = n O = 7,2 : 16 = 0,45 mol
Từ phương trình ta có:
n HCl = 2 n H 2 O = 2.0,45 = 0,9 mol
⇒ V HCl = 0,9/0,4 = 2,25l

Ta có sơ đồ chuyển hoá :
Mg, Zn, Al → O 2 MgO, ZnO, Al 2 O 3
MgO + 2HCl → MgCl 2 + H 2 O
ZnO + 2HCl → ZnCl 2 + H 2 O
Al 2 O 3 + 6HCl → 2 AlCl 3 + 3 H 2 O
MgO, ZnO, Al 2 O 3 → HCl MgCl 2 , ZnCl 2 , AlCl 3
Bảo toàn khối lượng: m oxit + m HCl = m muối + m H 2 O
⇒ 20,3 + 0,9.36,5 = m muối + 0,45.18
⇒ m muối = 45,05g


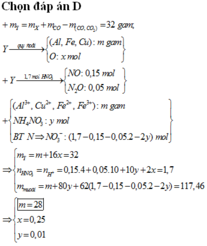
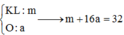
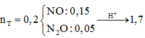
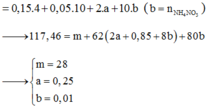




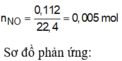

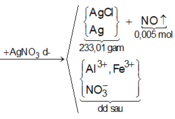

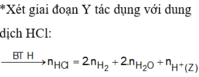


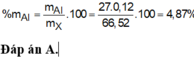

Coi hỗn hợp Y gồm :
Kim loại : 14,3(gam)
O :(x mol)
\(2H^+ + O^{2-}\to H_2O\\ 2H^+ + 2e \to H_2\)
Ta có : \(n_{Cl^-} = n_{HCl} = n_{H^+} = 2n_O + 2n_{H_2} = 2x + 0,4(mol)\)
Mà :
\(m_{muối} = m_{kim\ loại} + m_{Cl^-} = 14,3 + (2x + 0,4).35,5 = 49,8(gam)\\ \Rightarrow x = 0,3\)
Vậy : \(a = m_{kim\ loại} + m_O = 14,3 + 0,3.16 = 19,1(gam)\)