Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Fe+Cu\left(NO_3\right)_2->Fe\left(NO_3\right)_2+Cu\\ \Delta m=0,1x\left(64-56\right)=0,8\\ x=1\left(M\right)\)
Gọi a là số mol Cu(NO3)2 tham gia phản ứng
Phương trình hóa học:
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
a ← a → a a mol
Theo đề bài ta có: mCu bám vào – mFe tan ra = mKL tăng
64a – 56a = 0,8 a = 0,1
Nồng độ dung dịch Cu(NO3)2 là:
x = 0,1/0,1 = 1M.

a) $Fe + CuSO_4 \to FeSO_4 + Cu$
b)
Khối lượng thanh sắt tăng là $13,2 - 10 = 3,2(gam)$
Theo PTHH : $n_{Cu} = n_{Fe\ pư} = a(mol)$
$\Rightarrow 64a - 56a = 3,2$
$\Rightarrow a = 0,4(mol)$
$m_{Fe} = 0,4.56 = 22,4(gam)$
$m_{Cu} = 0,4.64 = 25,6(gam)$
$c) n_{CuSO_4} = n_{Fe} = 0,4(mol)$
$\Rightarrow C_{M_{CuSO_4}} = \dfrac{0,4}{0,2} = 2M$

n C U S O 4 = x.0,2 mol
F e + C u S O 4 → F e S O 4 + C u
x.0,2 x.0,2 x.0,2 (mol)
Khi nhúng thanh Fe vào dung dịch C u S O 4 , thanh Fe lúc sau có khối lượng tăng lên 1,6 gam là:
m C u b a m v a o - m F e tan = 1,6 g
⇔ 0,2x.64 - 0,2x.56 = 1,6
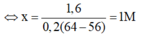
⇒ Chọn C.
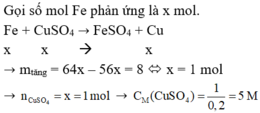
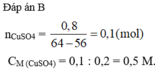
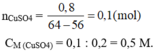

( Không chắc nhé :)))
\(n_{Cu\left(NO_3\right)_2}=0,02.0,3=0,006\left(mol\right)\)
\(PTHH:Fe+Cu\left(NO_3\right)_2\rightarrow Fe\left(NO_3\right)_2+Cu\)
\(\left(mol\right)\) `0,006` `0,006` `0,006`
\(\Delta m\uparrow=0,006.64-0,006.56=0,048\left(g\right)\)
\(m_{vb}=45+0,048=45,048\left(g\right)\)