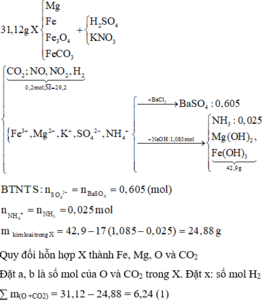
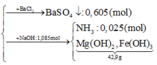
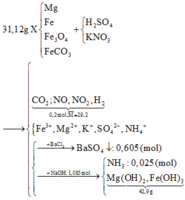
Hòa tan hết 31,12 gam hỗn hợp X gồm Mg, Fe (a mol), F e 3 O 4 , F e C O 3 vào dung dịch hỗn hợp chứa H 2 S O 4 và K N O 3 . Sau phản ứng thu được 1,12 lít hỗn hợp khí Y (đo ở 0oC và 4 atm) gồm ( C O 2 , NO, N O 2 , H 2 ) có tỷ khối hơi so với H 2 là 14,6 và dung dịch Z chỉ chứa các muối trung hòa với tổng khối lượng là m gam. Cho B a C l 2 dư vào Z thấy xuất hiện 140,965 gam kết tủa trắng. Mặt khác cho NaOH (dư) vào Z thì thấy có 54,25 gam dung dịch NaOH 80% phản ứng đồng thời xuất hiện 42,9 gam kết tủa và 0,56 lít khí (đktc) thoát ra. Biết các phản ứng xảy ra hoàn toàn. Giá trị của a gần nhất với:
A. 0,171
B. 0,165
C. 0,152
D. 0,159

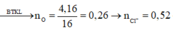
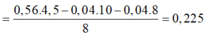


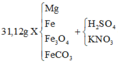
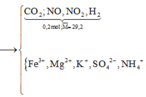
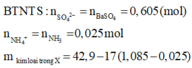 = 24,88 gam
= 24,88 gam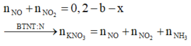

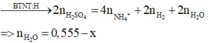
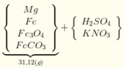
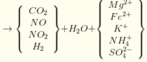
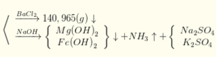
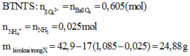
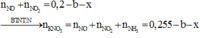
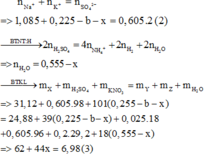
Đáp án D
n h h k h i = 0 , 2 m o l
cho BaCl2 vào kết tủa thu được là BaSO4
n B a S O 4 = 0 , 605 m o l
n H 2 S O 4 = 0 , 605 m o l
n N a O H = 1 , 085 m o l
n N H 3 = 0 , 025 m o l
⇒ n i o n k i m l o a i = 1 , 06 m o l
hỗn hợp khí có chứa H2 nên muối sắt là muối Fe2+
NO3- hết, các muối trung hòa là
MgSO4, FeSO4, K2SO4 và (NH4)2SO4
m F e + m M g = 24,88 gam (1)
nđiện tích - = 2nSO42-= 1,21 mol
nđiện tích += 1,085 + n K +
=> n K + = 0,125 mol
=>nN khí = 0,125 – 0,025 =0,1 mol
Mặt khác bảo toàn khối lượng
m X + m H 2 S O 4 + m K N O 3 = m m u ố i + m k h í + m H 2 O
=> m H 2 O = 8,91 mol
=> n H 2 O = 0,495 mol
Bảo toàn nguyên tố H có
nH axit = nH ( H 2 O )+ nH ( H 2 ) +nH muối amoni
0,605.2 =0,495.2 +2 n H 2 + 0,025.4
=> n H 2 = 0,06 mol
=> n C O 2 = 0,2 – 0,1 – 0,06 = 0,04 mol
=> n F e C O 3 = 0,04 mol
=> mFe + mMg + m F e 3 O 4 = 26,48 g
m KL (hỗn hợp trên)= 22,64 gam (2)
từ (1) và (2) => mO ( F e 3 O 4 )= 3,84 gam
=> n F e 3 O 4 =0,06 mol
mặt khác vì tổng ion dương kim loại F e 2 + v à M g 2 +
Gọi n F e = a m o l , n M g = b m o l
⇒ 2 a + 2 b = 0 , 2 56 a + 24 b = 12 , 56
⇒ a = 0 , 16 , b = 0 , 15 m o l