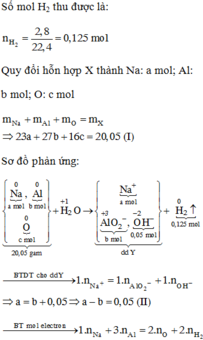
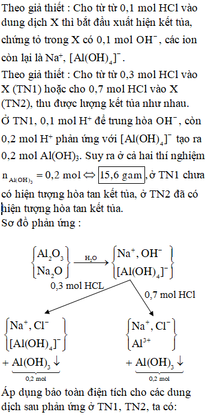
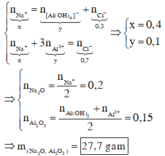
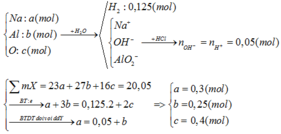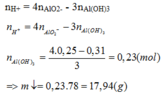Hỗn hợp X gồm Na, Al, Na2O và Al2O3. Hòa tan hoàn toàn 20,05 gam X vào nước, thu được 2,8 lít khí H2 (đktc) và dung dịch Y. Thêm từ từ dung dịch HCl 1M vào Y, đến khi bắt đầu xuất hiện kết tủa thì dùng hết 50ml, nếu thêm tiếp 310ml nữa thì thu được m gam kết tủa. Giá trị của m là
![]()
![]()
![]()
![]()