Cho m gam hỗn hợp gồm một kim loại kiềm M và Al vào nước dư thu được dung dịch A; 0,4687m gam chất rắn không tan và 7,2128 lít H2 (đktc). Cho từ từ dung dịch HCl có số mol lớn hơn 0,18 mol vào dung dịch A, ngoài kết tủa còn thu được dung dịch B. Cô cạn dung dịch B thu được 11,9945gam chất rắn khan. Giá trị m gần nhất với giá trị nào sau đây?
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Những câu hỏi liên quan

14 tháng 12 2019
Đáp án C
Các phản ứng xảy ra:
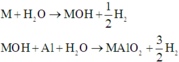
Vì dung dịch X chứa hai chất tan nên hai chất tan đó là MOHvà MA1O2.
Khi đó cả M và Al đều tan hết.
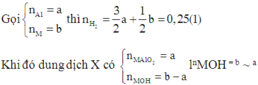
Vì lượng kết tủa thu được là lớn nhất nên
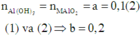
Mặt khác mAl + mM = 10,5 hay 0,1.27 + 0,2. ⇔ M = 10,5 M = 39 là K.

15 tháng 4 2022
bn check xem khối lượng mol M' bằng 1,793 hay 1,739 khối lượng mol M ?
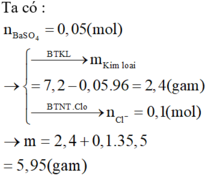

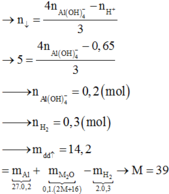
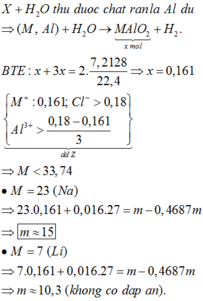


Đáp án C
M + H2O -> MOH + ½ H2
MOH + Al + H2O -> MAlO2 + 3/2H2
Do còn chất rắn không tan => Al dư
=> nM = nMAlO2 = 1/2nH2 = 0,161 mol
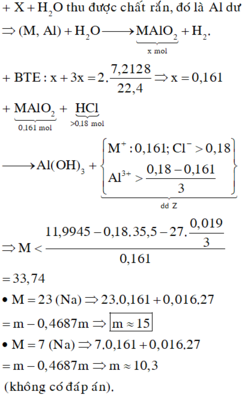
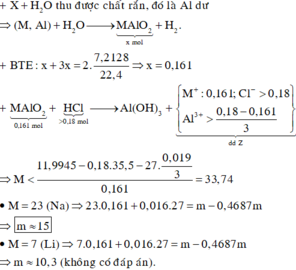
MAlO2 + HCl -> MCl + Al(OH)3
,nHCl = x > 0,18 mol => nAl(OH)3 = 1/3 (4nAlO2 – nH+) = (0,644 – x)/3
Và nAlCl3 = 1/3(nHCl – nAlO2) = (x – 0,161)/3 mol ; nMCl = nMAlO2 = 0,161 mol
=> mAlCl3 + mMCl = 11,9945g = 44,5(x – 0,161) + 0,161.(M + 35,5)
=> 44,5x + 0,161M = 13,4435
Do x > 0,18 => M < 33,75 => M là Na ( Li không tan nhiều trong nước)
=> nNa = 0,161 và nAl pứ = 0,161
=> m – 0,4687m = 0,161.23 + 0,161.27 => m = 15,15g
=>C