Một loại nước tự nhiên có chứa [Ca2+] = 4.10-4M; [HCO3-] = 3.10-4M, còn lại là ion Cl-. Để làm mềm loại nước này thường có 2 cách
- Cách 1: Cho tác dụng với lượng vừa đủ Na2CO3
- Cách 2: Cho tác dụng vừa đủ với CaO để loại bỏ phần nước cứng tạm thời rồi sau đó tác dụng vừa đủ với Na2CO3
Một nhà máy sản xuất nước sinh hoạt có công suất trung bình 100000 m3/1 ngày đêm, dùng nguồn nước trên để sản xuất nước sạch (giả thiết là nước mất hoàn toàn độ cứng) nếu sử dụng cách 2 thì 1 năm (365 ngày) nhà máy nước này sẽ tiết kiệm được so với cách 1 bao khoảng nhiêu tiền? (biết đơn giá Na2CO3: 6000đ/1kg; CaO; 1000đ/1kg)



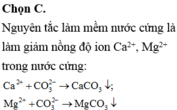
Đáp án : C
+) Cách 1 :
Xét 1 lit nước => nCa2+ = nNa2CO3 = 4.10-4 mol
=> trong 1 ngày thì : mNa2CO3 = 106.4.10-4.100000 = 4,24 kg
=> Thành tiền = 25,44 triệu đồng
+) Cách 2 :
Xét 1 lit nước
CaO + H2O -> Ca(OH)2
OH- + HCO3- -> CO32- + H2O
Ca2+ + CO32- -> CaCO3
=> nCaO = ½ nHCO3 = 1,5.10-4 mol
=> nCa2+ còn = 4.10-4 + 1,5.10-4 – 3.10-4 = 2,5.10-4 mol
=> nCa2+ = nNa2CO3 = 2,5.10-4 mol
=> trong 1 ngày thì :
mNa2CO3 = 106.2,5.10-4.100000 = 2,65 kg
, mCaO = 56. 1,5.10-4.100000 = 0,84 kg
=> Thành tiền = 16,74 triệu đồng
Trong 1 năm tiết kiệm được : 365.(25,44 – 16,74) = 3175,5 triệu đồng