Hỗn hợp X gồm 3 axit đơn chức mạch hở trong đó có hai axit no là đồng đẳng kế tiếp và một axit không no có một liên kết đôi. Cho m gam X tác dụng với dung dịch chứa 0,7 mol NaOH. Để trung hòa lượng NaOH dư cần 200ml dung dịch HCl 1M và thu được dung dịch D. Cô cạn cẩn thận D thu được 52,58 gam chất rắn khan E. Đốt cháy hoàn toàn E rồi hấp thụ toàn bộ sản phẩm khí và hơi vào bình đựng dung dịch NaOH dư thấy khối lượng bình tăng 44,14 gam. Thành phần % khối lượng axit không no là
A. 44,89
B. 48,19
C. 40,57
D. 36,28

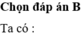
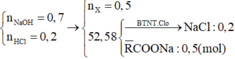
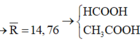
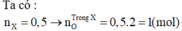

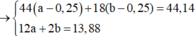
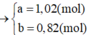
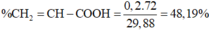
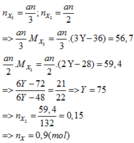
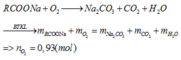
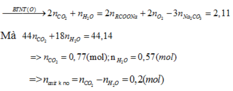
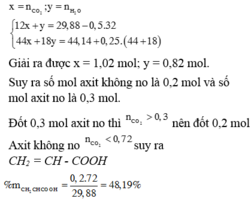
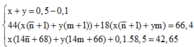
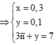
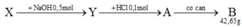

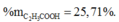
Đáp án : B
Đặt công thức cho 2 axit no và axit không no: CnH2nO2 (a mol) và CmH(2m-2)O2 (b mol)
Trong rắn có NaCl 0,2 mol và a + b = 0,5 (mol)
Ta có m(2 axit) = 52,58 - 0,2.58,5 - 0,5.22 = 29,88 (g)
Viết pt:
2CnH(2n-1)O2Na + (3n-2)O2 ---> (2n-1)CO2 + ((2n-1)H2O + Na2CO3
a -> a.(3n-2)/2
2CnH(2n-3)O2Na + (3n-3)O2 ---> (2n-1)CO2 + ((2n-3)H2O + Na2CO3
b -> b.(3n-3)/2
Ta có tổng khối lượng muối axetat là: 52,58 - 0,2.58,5 = 40,88g
=> tổng khối lượng CO2 và H2O là: 44,14g
=> khối lượng Na2CO3: 0,25.106 = 26,5g
=> Bảo toàn khối lượng suy ra khối lượng O2 phản ứng: 44,14 + 26,5 - 40,88 = 29,76g
=> Số mol O2 = (3an + 3bm - 2a - 3b)/2 = 0,93 (1)
Lại có m(2 axit) = a.(14n +32) + b.(14m + 30) = 29,88g (2)
Từ (1) và (2) => (124/3).a + 44b = 21,2
Kết hợp với phương trình ban đầu: a + b = 0,5
Ta được: a = 0,3mol và b = 0,2mol
Thế a, b vừa tìm được vào pt (1) được: 0,9n + 0,6m = 3,06
Tới đây ta biện luận do axit không no 1 nối đôi nên m ≥ 3
Với m > 3 thì n < 1 => loại => m = 3 và n = 1,4 => Công thức các axit: HCOOH, CH3COOH, CH2=CHCOOH => %maxit ko no = 0,2.72/29,88 = 48,19%