Đốt cháy hoàn toàn m gam hỗn hợp hai ancol no, đơn chức, mạch hở. Sau phản ứng thu được 15,68 lít khí CO2 ở đktc và 18 gam nước. Giá trị của m là:
A. 15,2 gam
B. 10,4 gam
C. 16,6 gam
D. 12,8 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Lời giải
n C O 2 = 0 , 9 ( m o l ) ; n H 2 O = 1 , 05 ( m o l ) ⇒ ancol phải no, mạch hở
Vì X gồm axit no, đơn chức, mạch hở, khi đốt cháy thu được
⇒ n H 2 O - n C O 2 = 0 , 15 ( m o l )
Để tính được khối lượng este ta phải tính được số mol axit, ancol và công thức của axit, ancol. Trước tiên ta đi tìm số mol axit. Ta thấy ta đã biết axit đơn chức =>1 nguyên tử axit có 2 nguyên tử O => ta chỉ cần tính số mol O trong axit
Bảo toàn khối lượng ta có:
m X = m C + m H + m O t r o n g X ⇒ m O t r o n g X = 21 , 7 - 12 n C O 2 - 2 n H 2 O = 8 , 8 ( g ) ⇒ n O t r o n g X = 0 , 55 ( m o l ) L ạ i c ó : n O t r o n g a n c o l = 0 , 15 ( m o l ) ⇒ n O t r o n g a x i t = 0 , 4 ( m o l ) ⇒ n a x i t = 0 , 2 ( m o l )
Gọi số nguyên tử C trong phân tử axit, ancol lần lượt là x, y
⇒ n C O 2 = 0 , 2 x + 0 , 15 y = 0 , 9 ⇒ 4 x + 3 y = 18
Ta dễ dàng suy ra x = 3; y = 2
axit là C2H5COOH; ancol là C2H5OH este là C2H5COOC2H5
Ta thấy nancol < naxit phản ứng tính theo số mol ancol
⇒ n e s t e = 60 % n a n c o l = 0 , 09 ( m o l )
Vậy meste = 9,18(g)
Đáp án A.

Chọn đáp án A
• 16 , 6 g a m h h G g ồ m C n H 2 n O 2 v à R - O H + O 2 → 0 , 7 m o l C O 2 + 0 , 9 m o l H 2 O
Vì n H 2 O > n C O 2 → ancol no, đơn chức
→ nancol = 0,9 - 0,7 = 0,2 mol.
Giả sử có x mol axit; ancol có dạng CmH2m + 2O.
mG = mC + mH + mO
→ ( 2 x + 0 , 2 ) x 16 = 16 , 6 - 0 , 7 x 12 - 0 , 9 x 2
→ x = 0,1 mol.
n C O 2 = 0 , 1 n + 0 , 2 m = 0 , 7
→ n + 2m =7.
Biện luận → n = 1;
m = 3 thỏa mãn (Maxit < Mancol)
• 0,1 mol HCOOH và 0,2 mol C3H7OH vào H2SO4 đặc.
Theo lý thuyết meste = 0,1 x 88 = 8,8 gam
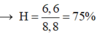

Đáp án A
• 16,6 gam hhG gồm CnH2nO2 và R-OH + O2 → 0,7 mol CO2 + 0,9 mol H2O
Vì nH2O > nCO2 → ancol no, đơn chức → nancol = 0,9 - 0,7 = 0,2 mol.
Giả sử có x mol axit; ancol có dạng CmH2m + 2O.
mG = mC + mH + mO → (2x + 0,2) x 16 = 16,6 - 0,7 x 12 - 0,9 x 2 → x = 0,1 mol.
nCO2 = 0,1n + 0,2m = 0,7 → n + 2m =7.
Biện luận → n = 1; m = 3 thỏa mãn (Maxit < Mancol)
• 0,1 mol HCOOH và 0,2 mol C3H7OH vào H2SO4 đặc.
Theo lý thuyết meste = 0,1 x 88 = 8,8 gam
=> H=6,6/8,8=75%

Đáp án D
Đốt cháy hoàn toàn 21,7 gam X thu được 0,9 mol CO2 và 1,05 mol H2O.
Do số mol H2O > CO2 nên ancol là no.

Vậy axit là C2H5COOH còn ancol là C2H5OH.
Este tạo ra là C2H5COOC2H5 0,09 mol vậy m=9,18 gam

Đáp án : D
,nCO2 = 0,9 mol < nH2O = 1,05 mol
Vì axit no đơn chức => ancol đơ chức là ancol no
=> nancol = nH2O – nCO2 = 0,15 mol
Bảo toàn khối lượng : mX + mO2 = mCO2 + mH2O
=> nO2 = 1,15 mol
Bảo toàn O : 2naxit + nancol + 2nO2 = 2nCO2 + nH2O
=> naxit = 0,2 mol
Công thức của axit là CnH2nO2 và ancol là CmH2m+2O
=> mX = 0,2.(14n + 32) + 0,15.(14m + 18) = 21,7g
=> 4n + 3m = 18
=> n = 3 và m = 2 thỏa mãn
C2H5COOH + C2H5OH -> C2H5COOC2H5 + H2O
=> Hiệu suất tính theo ancol ( số mol ancol nhỏ hơn)
=> neste = nancol.60% = 0,09 mol
=> m = 9,18g

Đáp án : B
Ta có : Este + O2 à CO2 + H2O
Vì este no, đơn chức , mạch hở
=> nCO2 = nH2O = 48 , 4 44 = 1,1 mol
Bảo toàn khối lượng => meste + mO2 = mCO2 + mH2O
=> m = 1,1.(44 + 18) - 1,35.32 = 25 g
Đáp án A