Điện phân 500ml dung dịch hỗn hợp gồm FeCl3 0,4M và CuCl2 0,5M với điện cực trơ. Khi ở anot thoát ra 8,96 lít khí (đktc) thì khối lượng kim loại thu được ở catot là:
A. 21,60 gam
B. 18,60 gam
C. 18,80 gam
D. 27,84 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Các ion tham gia điện phân ở catot theo thứ tự tính oxi hóa từ mạnh đến yếu (Fe3+ > Cu2+ > H+ > Fe2+).
Khi ở catot bắt đầu thoát khí (tức H+ chỉ mới bắt đầu điện phân)
=> Fe3+ chỉ bị khử thành Fe2+ và Cu2+ bị khử hoàn toàn) => n(e trao đổi)=0,1.2+0,2.1=0,4
=> n(Cl2 ) = 0,2 => V = 4,48 (lít) => Đáp án B

Chọn đáp án B
Dung dịch X bị điện phân đến khi xuất hiện bọt khí ở catot thì dừng ⇒ Cu2+ đã điện phân hết và catot chỉ còn H+ ⇒ Y chỉ chứa HNO3, còn 2 khí có số mol 0,44 mol tại anot là Cl2 và O2


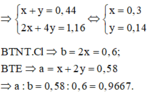
Chọn C
Catot :
Fe3+ + 1e -> Fe2+
Cu2+ + 2e -> Cu
Fe2+ + 2e -> Fe
Anot : 2Cl- -> Cl2 + 2e
2H2O -> 4H+ + O2 + 4e
,nFe3+ = 0,2 mol ; nCu2+ = 0,25 mol ; nCl = 1,1 mol
nkhí = 0,4 mol < ½ nCl ( Cl- dư) => ne = 0,4.2 = 0,8 mol
=> sau phản ứng có : 0,25 mol Cu và 0,05 mol Fe
=> mKL = 18,8g