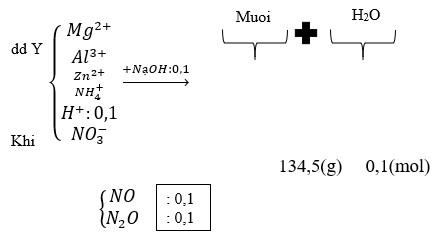
Hòa tan hoàn toàn 9,48 gam hỗn hợp Fe và FeO vào V (ml) dung dịch HNO3 0,5M. Sau khi phản ứng xảy ra hoàn toàn thì thu được dung dịch B và 3813 ml khí không màu (duy nhất) hóa nâu ngoài không khí, thể tích khí đo ở nhiệt độ 27°C, áp suất 1atm. Thể tích V (ml) của dung dịch HNO3 cần dùng là?
A. 910 ml
B. 1812 ml
C. 990 ml
D. 1300 ml








pV = nRT với p = 1atm; V = 3,813 lít;
R = 0,082; T = 273 + 27 = 300K.
khí hóa nâu ngoài không khí là NO
⇒ thay số có nNO = 0,155 mol.
phản ứng xảy ra hoàn toàn nên Fe sẽ lên Fe3+ trong muối Fe(NO3)3.
Bảo toàn electron có: 3nFe + nFeO = 3nNO = 0,465 mol.
Lại có: mFe + mFeO = 9,48 gam
⇒ giải nFe = 0,15 mol; nFeO = 0,015 mol.
⇒ ∑nFe(NO3)3 = 0,165 mol
⇒ bảo toàn N có ∑nHNO3 cần = 0,65 mol.
⇒ VHNO3 = 0,65 ÷ 0,5 = 1,3 lít = 1300 mL
Đáp án D