Đốt cháy 6g khí X gồm Al, Fe, Zn trong oxi, sau 1 thời gian thu đc 8,08g chất rắn Z gồm oxit kim loại và kim loại còn dư . Tính thể tích khí oxi ( đktc) đã phán ứng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1./ Dẫn luồng khí H2 qua ống đựng CuO:
CuO + H2 → Cu + H2O
a a a
Khối lượng chất rắn giảm:
Δm = m(CuO pư) - m(Cu) = 80a - 64a = 80 - 72,32 = 7,68g
⇒ a = 7,68/16 = 0,48g
Số mol H2 tham gia pư: n(H2) = 0,48/80% = 0,6mol
Theo ĐL bảo toàn nguyên tố, số mol HCl tham gia pư là: n(HCl pư) = 2.n(H2) = 1,2mol
Theo ĐL bảo toàn khối lượng:
m(hh rắn) + m(HCl pư) = m(muối) + m(H2) ⇒ m(muối) = m(hh rắn) + m(HCl pư) - m(H2)
⇒ m(muối) = 65,45 + 0,12.36,5 - 0,6.2 = 108,05g
Gọi x, y là số mol Al và Zn có trong hh KL ban đầu.
m(hh KL) = m(Al) + m(Zn) = 27x + 65y = 40,6g
m(muối) = m(AlCl3) + m(ZnCl2) = 133,5x + 136y = 108,05g
⇒ x = 0,3mol và y = 0,5mol
Khối lượng mỗi kim loại:
m(Al) = 0,3.27 = 8,1g; m(Zn) = 65.0,5 = 32,5g
Thành phần % khối lượng mỗi kim loại:
%Al = 8,1/40,6 .100% = 19,95%
%Zn = 32,5/40,6 .100% = 80,05%

Theo ĐLBT KL, có: mKL + mO2 = m oxit
⇒ mO2 = 28,4 - 15,6 = 12,8 (g)
\(\Rightarrow n_{O_2}=\dfrac{12,8}{32}=0,4\left(mol\right)\Rightarrow V_{O_2}=0,4.22,4=8,96\left(l\right)\)

a) Gọi số mol Al, Zn là 2a, a (mol)
PTHH: 4Al + 3O2 --to--> 2Al2O3
2a-->1,5a---------->a
2Zn + O2 --to--> 2ZnO
a---->0,5a------->a
=> \(102a+81a=18,3\)
=> a = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{0,2.27+0,1.65}.100\%=45,378\%\\\%m_{Zn}=\dfrac{0,1.65}{0,2.27+0,1.65}.100\%=54,622\%\end{matrix}\right.\)
b) \(n_{O_2}=1,5a+0,5a=0,2\left(mol\right)\)
=> \(V_{O_2}=0,2.22,4=4,48\left(l\right)\)

a, 2Mg + O2 \(\underrightarrow{t^o}\) 2MgO
b, \(n_{Mg}=\dfrac{4,8}{24}=0,2mol\)
\(n_{O_2}=\dfrac{0,2}{2}=0,1mol\)
\(m_{O_2}=0,1.32=3,2g\)
\(V_{O_2}=0,1.22,4=2,24l\)
c, Cách 1:
\(Theo.ĐLBTKL,ta.có:\\ m_{Mg}+m_{O_2}=m_{MgO}\)
\(\Rightarrow m_{MgO}=4,8+3,2=8g\)
Cách 2:
\(n_{MgO}=\dfrac{0,2.2}{2}=0,2mol\)
\(\Rightarrow m_{MgO}=0,2.40=8g\)

Bảo toàn khối lượng :
m O = 80 - 72,32 = 7,68 gam
n O = 7,68/16 = 0,48(mol)
$H_2 + O_{oxit} \to H_2O$
n H2 pư = n O = 0,48(mol)
=> n H2 = 0,48/80% = 0,6(mol)
Gọi n Al = a(mol) ; n Zn = b(mol)
=> 27a + 65b = 40,6 (1)
Bảo toàn khối lượng :
n Cl2 pư = 65,45 - 40,6 = 24,85(gam)
n Cl2 = 24,85/71 = 0,35(mol)
Bảo toàn electron :
3n Al + 2n Zn = 2n Cl2 + 2n H2
<=> 3a + 2b = 0,35.2 + 0,6.2(2)
Từ (1)(2) suy ra a = 0,3 ; b = 0,5
%m Al = 0,3.27/20,6 .100% = 20%
%m Fe = 100% -20% = 80%
Làm sao biết bảo toàn electron đó như nào ạ??
3nAl +2nZn=... đó ạ

Kim loại không tan là Cu dư.
Cu dư => Muối thu được gồm FeCl2 và CuCl2 vì: Cu + 2FeCl3 → CuCl2 + 2FeCl2
Số mol các chất là: 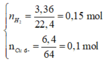
Sơ đồ phản ứng:
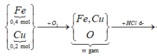
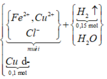
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Đáp án A.