Công thức phân tử của hợp chất khí tạo bởi nguyên tố R và hiđro là RH3. Trong oxit mà R có hoá trị cao nhất thì oxi chiếm 74,07% về khối lượng. Nguyên tố R là
A. S
B. N
C. P
D. As
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn A
Công thức oxit ứng với hóa trị cao nhất của R là R 2 O 5
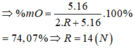
Dạ cho em hỏi là 74,07 phần trăm suy ra như thế nào vậy ạ? Em cảm ơn.

Đáp án A
Hướng dẫn %R = 100% - %O = 100% - 74,07% = 25,93%
Hợp chất khí với Hidro là RH3 => b = 3
a + b = 8 => a = 5
Công thức Oxit cao nhất là R2O5
![]() = 2.MR =
= 2.MR = ![]() <=> 2.MR = 28 <=> MR =
<=> 2.MR = 28 <=> MR = ![]() = 14 => R là Nitơ
= 14 => R là Nitơ

Hợp chất khí của R với hiđro có công thức phân tử là RH3.
Hợp chất oxit cao nhất của nguyên tố R là R2O5
Ta có \(\%O=\dfrac{16.5}{2R+16.5}.100=56,34\\ \Rightarrow R=31\left(Photpho-P\right)\\ \Rightarrow Z_R=SốE=15\)

Công thức hoá học các hợp chất với oxi và hiđro là CO 2 và CH 4

Chọn B.
Công thức với H là RH3 nên công thức oxit cao nhất là R2O5.
Ta có: %R = 43,66% => %O = 56,34%. Do đó:
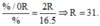
Vậy R là P (photpho).
Đáp án : B
Qui tắc bát tử : Do số hóa trị trong hợp chất với H là 3
=> Số hóa trị trong hợp chất oxit cao nhất là 8 – 3 = 5
=> R2O5 => %mO(oxit) = 5 . 16 2 R + 5 . 16 . 100 % = 74 , 07 %
=> R = 14 (N)
=> B
N