Giá trị pH của dung dịch HCl 0,01M là
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan
NH
1
NH
1

18 tháng 4 2017
Đáp án D
nOH- = 0,01.2 = 0,02
nH+ = 0,2 . 0,04 = 0,008
⇒ Trong dung dịch B có nOH- = 0,02 – 0,008 = 0,012
VB = 1,2 . 10 = 12l ⇒ [OH-] = 0,001
⇒ pH = 11
DM
3


3 tháng 12 2019
nH+=nHCl=0,2.0,04=0,008(mol)
nOH-=1.0,01.2=0,02(mol)
\(\rightarrow\)nOH- dư=0,012(mol)
CM(OH-)=\(\frac{0,012}{1,2}\)=0,01(M)
Pha loãng 10 lần nên CM[OH-]=0,001(M)
pH=14-pOH=14-[-log(0,001)]=11



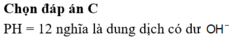
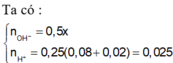
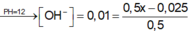
pH = -log[H+] = -log(0,01) = 2
Đáp án A