Cho các cân bằng hóa học sau
(1) H 2 + I 2 ⇔ 2 H I
( 2 ) 1 2 H 2 + 1 2 I 2 ⇔ H I
(3) 2 H I ⇔ H 2 + I 2
Với lần lượt các giá trị hằng số cân bằng K c b 1 , K c b 2 , K c b 2 . Nhận định nào sau đây đúng
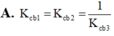
![]()
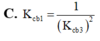
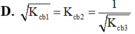
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1 :
b)
Cho quỳ tím ẩm vào mẫu thử
- mẫu thử hóa đỏ là P2O5
P2O5 + 3H2O $\to$ 2H3PO4
- mẫu thử hóa xanh là Na2O,CaO
Na2O + H2O $\to $ 2NaOH
CaO + H2O $\to$ Ca(OH)2
- mẫu thử không đổi màu là NaCl
Cho hai mẫu thử còn vào dung dịch H2SO4
- mẫu thử tạo kết tủa trắng là CaO
CaO + H2SO4 $\to$ CaSO4 + H2O
- mẫu thử không hiện tượng là Na2O
Câu 2 :
1)
\(S_{Na_2SO_4} = \dfrac{m_{Na_2SO_4}}{m_{H_2O}}.100 = \dfrac{7,2}{80}.100\% = 9(gam)\\ C\%_{Na_2SO_4} = \dfrac{S}{S + 100}.100\% = \dfrac{9}{100 + 9}.100\% = 8,26\%\)

HD:
a)
FeS - 9e = Fe+3 + S+6
N+5 + 3e = N+2
------------------------------------
FeS + 3N+5 = Fe+3 + S+6 + 3N+2
FeS + 6HNO3 ---> Fe(NO3)3 + H2SO4 + 3NO + 2H2O
b)
Fe+3 + e = Fe+2
2I- -2e = I2
-------------------------
2Fe+3 + 2I- = 2Fe+2 + I2
2FeCl3 + 2KI ---> 2FeCl2 + I2 + 2KCl

Câu 1: Hóa trị của Fe trong hai hợp chất FeCl3, FeCl2 là:
A. I
B. III, II
C. I, III
D. I, II
Câu 2: Cho các kí hiệu và các công thức hóa học: Cl, H, O, C, CO2, Cl2, H2, O2. Dãy gồm các đơn chất là:
A. Cl, H, O, C
B. CO2, Cl2, H2, O2
C. C, Cl2, H2, O2
D. CO2, Cl, H, O2
Câu 3: Các nguyên tử của cùng một nguyên tố hóa học có cùng
A. khối lượng
B. số proton
C. số nơtron
D. cả A, B, C
Câu 4: Công thức hóa học dung để biểu diễn:
A. hợp chất
B. chất
C. đơn chất
D. hỗn hợp
Câu 5: Một kim loại M tạo muối sunfat M2(SO4)3. Muối nitrat của kim loại M là:
A. M(NO3)3
B. M2(NO3)2
C. MNO3
D. M2NO3
Câu 6: Trong nguyên tử luôn có:
A. số proton bằng số nơtron
B. số proton bằng số electron
C. số nowtron bằng số electron
D. số proton bằng số electron bằng số nơtron
Câu 1 :
\(2Al+3S\underrightarrow{^{^{t^0}}}Al_2S_3\)
\(FeCl_3+3NaOH\rightarrow Fe\left(OH\right)_3+3NaCl\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{^{^{t^0}}}FeCl_3\)
Câu 2 : Cái này có sẵn dạng trình bày trong SGk, anh chỉ ghi CT thoi nhé !
\(CaO,AlCl_3,\)
Câu 3 :
\(M_{H_2O}=2+16=18\left(\dfrac{g}{mol}\right)\)
\(M_{Al_2O_3}=24\cdot2+16\cdot3=102\left(\dfrac{g}{mol}\right)\)
\(M_{Mg_3\left(PO_4\right)_2}=24\cdot3+\left(31+64\right)\cdot2=262\left(\dfrac{g}{mol}\right)\)
\(M_{Ca\left(OH\right)_2}=40+17\cdot2=74\left(\dfrac{g}{mol}\right)\)

Tóm tắt:
\(S=5km\)
Người thứ nhất:
\(v_1=48km\)/h
\(v_2=60km\)/h
\(S_1=S_2=\dfrac{S}{2}\)
Người thứ hai:
\(v_1=48km\)/h
\(v_2=60km\)/h
\(t_1=t_2=\dfrac{t}{2}\)
So sánh \(v_{tb1}\) và \(v_{tb2}\)
--------------------------------------
Bài làm:
*Người thứ nhất:
Thời gian người đó đi trên nữa quãng đường đầu là:
\(t_1=\dfrac{S_1}{v_1}=\dfrac{S}{2\cdot v_1}=\dfrac{S}{2\cdot48}=\dfrac{S}{96}\left(h\right)\)
Thời gian người đó đi trên nữa quãng đường sau là:
\(t_2=\dfrac{S_2}{v_2}=\dfrac{S}{2\cdot v_2}=\dfrac{S}{2\cdot60}=\dfrac{S}{120}\left(h\right)\)
Vận tốc của người đó trên cả quãng đường là:
\(v_{tb1}=\dfrac{S}{t_1+t_2}=\dfrac{S}{S\cdot\left(\dfrac{1}{96}+\dfrac{1}{120}\right)}=\dfrac{1}{\dfrac{1}{96}+\dfrac{1}{120}}\approx53,33km\)/h
Người thứ hai:
Quãng đường người đó đi trên nữa thời gian đầu là:
\(S_1=v_1\cdot t_1=v_1\cdot\dfrac{t}{2}=\dfrac{48t}{2}=24t\left(km\right)\)
Quãng đường người đó đi trên nữa thời gian sau là:
\(S_2=v_2\cdot t_2=v_2\cdot\dfrac{t}{2}=\dfrac{60t}{2}=30t\left(km\right)\)
Vận tốc của người đó trên cả quãng đường là:
\(v_{tb2}=\dfrac{S_1+S_2}{t}=\dfrac{24t+30t}{t}=\dfrac{t\cdot\left(24+30\right)}{t}=24+30=54km\)/h
Vì \(v_{tb2}>v_{tb1}\) nên người thứ hai đến B trước người thứ nhất
Người 1 : \(v_{tb}=\dfrac{s_1+s_2}{t_1+t_2}=\dfrac{s+s}{\dfrac{s}{v_1}+\dfrac{s}{v_2}}=\dfrac{2s}{\dfrac{s}{v_1}+\dfrac{s}{v_2}}=\dfrac{2}{\dfrac{1}{v_1}+\dfrac{1}{v_2}}=\dfrac{2}{\dfrac{1}{48}+\dfrac{1}{60}}\approx53,33\left(km/h\right)\)Người 2 :
\(v_{tb}=\dfrac{s_1+s_2}{t_1+t_2}=\dfrac{v_1t+v_2t}{t+t}==\dfrac{48t+60t}{2t}=54\left(km/h\right)\)
Ta có : 53,33 < 54
Vậy người thứ hai đến B trước.


1. K(I) với CO3(II),
CTHH: K2CO3
PTK: 39.2 + 60 = 138 (đvC)
2. Al(III) với NO3(I)
CTHH: Al(NO3)3
PTK: 27 + 62.3 = 213 (đvC)
3. Fe(II) với SO4(II),
CTHH: FeSO4
PTK: 56+ 96 = 152 (đvC)
4. R(n) lần lượt với O(II).
CTHH: R2On
PTK : 2R + 16n ( đvC)

Trong kia k đánh Tiếng Việt được nên đánh TA nha :)
1. \(NaOH,Ba\left(OH\right)_2,H_2SO_4,H_2O\)
\(\left\{{}\begin{matrix}NaOH\\Ba\left(OH\right)_2\\H_2SO_4\\H_2O\end{matrix}\right.\underrightarrow{+qtims}\left\{{}\begin{matrix}Blue:NaOH,Ba\left(OH\right)_2\underrightarrow{+H_2SO_4}\left\{{}\begin{matrix}\downarrow:Ba\left(OH\right)_2\\\varnothing:NaOH\end{matrix}\right.\\Red:H_2SO_4\\Purple:H_2O\end{matrix}\right.\)
2.\(NaOH,HCl,BaCl_2,H_2O\)
\(C_1:\left\{{}\begin{matrix}NaOH\\HCl\\BaCl_2\\H_2O\end{matrix}\right.\underrightarrow{+qtim}\left\{{}\begin{matrix}Red:HCl\\Blue:NaOH\\Purplr:BaCl_2,H_2O\underrightarrow{+H_2SO_4}\left\{{}\begin{matrix}\downarrow:BaCl_2\\\varnothing:H_2O\end{matrix}\right.\end{matrix}\right.\)
câu1
Trích mẫu thử
cho quỳ tím vào các mẫu thử trên
+ dd làm quỳ tím chuyển thành màu xanh NaOH , Ba(OH)2
+ dd làm quỳ tím chuyển thành màu đỏ H2SO4
+ dd ko làm đổi màu quỳ tím H2O
cho H2SO4 vừa nhận biết vào NaOH và Ba(OH)2
+ dd xuất hiện kết tủa Ba(OH)2
Ba(OH)2 + H2SO4 =-------> BaSO4 +2 H2O
+ dd ko hiện tượng NaOH

1)
Cho các khí qua quỳ tím ẩm:
- Hóa đỏ: HCl
- Hóa hồng: CO2
Hai khí còn lại dẫn qua dd Br2 dư:
- Mất màu: C2H2
- Không ht: CH4
C2H2 + 2Br2 --> C2H2Br4
Chọn đáp án D
Khi viết công thức tính các hằng số cân bằng của các phản ứng thuận nghịch trên ta thấy