Điện phân (với điện cực trơ) 200 ml dung dịch CuSO4 nồng độ x mol/l, sau một thời gian thu được dung dịch Y vẫn còn màu xanh, có khối lượng giảm 8g so với dung dịch ban đầu. Cho 16,8g bột sắt vào Y, sau khi các phản ứng xảy ra hoàn toàn, thu được 12,4g kim loại. Giá trị của x là
A. 1,50
B. 3,25
C. 2,25
D. 1,25


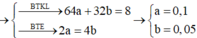
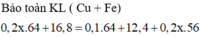


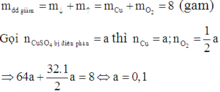
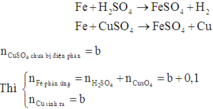
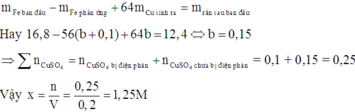

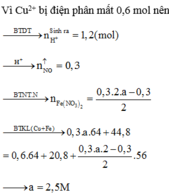


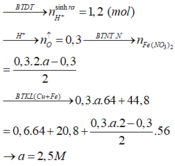
Đáp án : D
Catot : Cu2+ + 2e -> Cu2+
Anot : 2H2O -> 4H+ + O2 + 4e
Do dung dịch vẫn còn màu xanh nên Cu2+ dư
=> nH+ = 2nCu = 0,25 mol
Khi cho Fe vào thì :
Fe + 2H+ -> Fe2+ + H2
0,125 <- 0,25 mol
Fe + Cu2+ -> Fe2+ + Cu
.x <- x
=> mFe bđ – mKL sau = 56.(0,125 + x) – 64x = 16,8 – 12,4
=> x = 0,325 mol
=> nCu2+ bđ = 0,125 + 0,325 = 0,45 mol
=> CM (CuSO4) = 2,25M