Nhỏ rất từ từ dung dịch chứa HCl vào 100 ml dung dịch A chứa hỗn hợp các chất tan là NaOH 0,8M và K2CO3 0,6M. Lượng khí CO2 thoát ra được biểu di n trên đồ thị sau
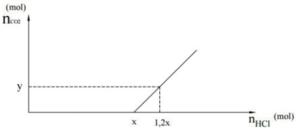
Giá trị của y trên đồ thị là
A. 0,028.
B. 0,014.
C. 0,016.
D. 0,024.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
nNaOH = 0,08 (mol) ; nK2CO3 = 0,06 (mol)
Nhỏ rất từ từ HCl vào dd NaOH và K2CO3 sẽ có phản ứng theo thứ tự:
H+ + OH- → H2O (1)
0,08 ← 0,08 (mol)
H+ + CO32- → HCO3- (2)
0,06←0,06 (mol)
H+ + HCO3- → CO2↑+ H2O (3)
Nhìn đồ thị ta thấy: giai đoạn bắt đầu xuất hiện khí thoát ra => nHCl = x (mol)
=> Lượng HCl này chính là lượng phản ứng ở (1) và (2)
=> x = 0,08 + 0,06 = 0,14 (mol)
Khí bắt đầu thoát ra đến khi nHCl = 1,2x (mol) => khi này phương trình (3) bắt đầu xảy ra
=> theo (3) nCO2 thoát ra = nHCl pư (3) = (1,2x –x) = 0,2x = 0,2.0,14 = 0,028 (mol)
=> chọn A

Đáp án A
PTHH:
H+ + OH- → H2O
0,08 0,08
H+ + CO32‑ → HCO3-
0,06 0,06
→ x = 0,14 → 1,2x = 0,168
H+ + HCO3- → CO2 + H2O
0,028 0,028

PTHH:
H+ + OH- → H2O
0,08 0,08
H+ + CO32‑ → HCO3-
0,06 0,06
→ x = 0,14 → 1,2x = 0,168
H+ + HCO3- → CO2 + H2O
0,028 0,028 → Đáp án A

Chọn D.
Ta có: x = 0,06 + 0,08 = 0,14 và y = 1,25x – 0,08 – 0,06 = 0,035

Đáp án D
Ta có: x = 0,06 + 0,08 = 0,14 và
y = 1,25x – 0,08 – 0,06 = 0,035

Đáp án A
+ Nhìn vào đồ thị : a + b + c = 0,3 và c = 0,4 – 0,3 = 0,1
+ Vậy a + b = 0,2

Đáp án B
![]()
Đồ thị trải qua các giai đoạn:
+Chưa xuất hiện kết tủa do NaOH trung hòa axit dư.
+Kết tủa tăng dần.
+Kết tủa giảm dần do NaOH hòa tan Al(OH)3, kết tủa sau cùng chỉ còn lại là Mg(OH)2.
Nhận thấy lúc 0,92 mol NaOH phản ứng thì kết tủa thu được là 0,18 mol Mg(OH)2
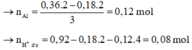
Giải được số mol H2SO4 0,16 mol, HCl 0,48 mol.
Cho V ml Ba(OH)2 0,4M và NaOH 0,8M chứa x mol Ba(OH)2 và 2x mol NaOH.
Để kết tủa hidroxit lớn nhất là 4x=0,08+0,12.3+0,18.2=0,8.
Để kết tủa BaSO4 lớn nhất là x>0,16.
Do vậy thỏa mãn x=0,2 suy ra V=0,5 lít=500ml.
Chọn đáp án A
nNaOH = 0,08 (mol) ; nK2CO3 = 0,06 (mol)
Nhỏ rất từ từ HCl vào dd NaOH và K2CO3 sẽ có phản ứng theo thứ tự:
H+ + OH- → H2O (1)
0,08 ← 0,08
H+ + CO32- → HCO3- (2)
0,06←0,06
H+ + HCO3- → CO2↑+ H2O(3)
Nhìn đồ thị ta thấy: giai đoạn bắt đầu xuất hiện khí thoát ra => nHCl = x (mol)
=> Lượng HCl này chính là lượng phản ứng ở (1) và (2)
=> x = 0,08 + 0,06 = 0,14 (mol)
Khí bắt đầu thoát ra đến khi nHCl = 1,2x (mol)
=> khi này phương trình (3) bắt đầu xảy ra
=> theo (3) nCO2 thoát ra = nHCl pư (3)
= (1,2x –x) = 0,2x = 0,2.0,14
= 0,028 (mol)