Cho phương trình phản ứng: Mg + HNO3 → Mg(NO3)2 + NO + N2O + H2O. Nếu tỉ khối của hỗn hợp NO và N2O đối với H2 là 19,2. Ti lệ số phân tử bị khử và bị oxi hóa là
A. 11 : 28
B. 8 : 15
C. 38 : 15
D. 6 : 11
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp ánA
Chọn 1 mol hỗn hợp khí NO và N2O.
Gọi

Theo định luật bảo toàn mol electron:
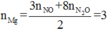
Áp dụng định luật bảo toàn nguyên tố cho nitơ có:
![]()
Vậy tỉ lệ số phân tử bị khử và bị oxi hóa trong phản
ứng là: ![]()

Đáp án A:
Chọn 1 mol hỗn hợp khí NO và N2O
Theo phương pháp đường chéo
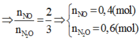
=>nN bị khử= 1,6 (mol)
![]()
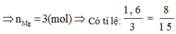

Chọn A
Theo bảo toàn electron và bảo toàn nguyên tố Mg, ta có
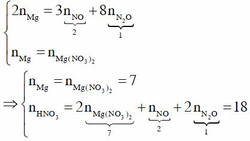

Đáp án : B
(3x + 8y) Al -> Al3+ + 3e
3 (x + 2y)N5+ + (3x + 8y) -> xN2+ + 2yN1+
=> số phân tử HNO3 bị khử = số N trong sản phẩm khử = 3(x + 2y) = 3x + 6y

Đáp án D
Số phân tử bị khử chính bằng số phân tử N2O
8Al + 30HNO3 (loãng) → 8Al(NO3)3 + 3N2O + 15H2O

Đáp án : A
Số phân tử bị khử chính bằng số phân tử N2O
8Al + 30HNO3 à 8Al(NO3)3 + 3N2O + 15H2O

Đáp án C
Số oxi hóa của các nguyên tố thay đổi:
F e + 8 / 3 3 O 4 + H N + 5 O 3 → F e + 3 ( N O 3 ) 3 + N + 2 O + H 2 O
Các quá trình nhường, nhận electron:
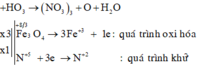
=> Tỉ lệ số phân tử bị oxi hóa : số phân tử bị khử = 3: l
Phương trình:
15 Mg + 38 HNO3 -> 15 Mg[NO3]2 + 2NO + 3 N2O + 19 H2O => ti lệ: (3.2 + 2)/15 = 8/15
=> Đáp án B