Cho 5,6 gam Fe vào 200 ml dung dịch Cu(NO3)2 0,5M và HCl 1,2 M thu được khí NO và m gam kết tủa. Xác định m. Biết rằng NO là sản phẩm khử duy nhất của NO3– và không có khí H2 bay ra
A. 0,64.
B. 2,4.
C. 0,3.
D. 1,6.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
Ta có nFe = 0,1 || nCu(NO2)2 = 0,1 || nHCl = 0,24
● Nhận thấy nH+ = 0,24 và nNO3– = 0,2 ⇒ nNO = 0,06
● Ta có 3nNO > 2nFe ⇒ Fe chỉ lên Fe2+.
⇒ nFe phản ứng với HNO3 = nNO × 3 ÷ 2 = 0,09 mol
⇒ nFe phản ứng với Cu2+ = 0,1 - 0,09 = 0,01 mol
⇒ m↓ = mCu = 0,01×64 = 0,64 gam ⇒ Chọn A

Chọn D
nFe = 0,1 ; nCu(NO3)2 = 0,1 ; nHCl = 0,2
Do nHCl < 8/3.nFe nên phản ứng chỉ tạo Fe2+
3Fe + 8H+ + 2NO3- -> 3Fe2+ + 2NO + 4H2O
=> Sau phản ứng còn lại : 0,1 – 0,075 = 0,025 mol
Fe + Cu2+ -> Fe2+ + Cu
=> m = mCu = 64.0,025 = 1,6g

n(Fe) = 0,1 mol; n(Cu(NO3)2) = 0,1 mol; n(HCl) = 0,2 mol
PTHH:
3Fe + 8H+ + 2NO3- → 3Fe2+ + 2NO + 4H2O
0,075
Fe + Cu2+ → Fe2+ + Cu
0,025 0,025 mol → m(Cu) = 1,6 gam → Đáp án A

Chọn đáp án A
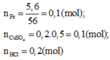
Do sau phản ứng thu được m gam chất rắn( chính là Cu) nên Fe chỉ tạo muối Fe2+
3Fe + 2NO3- + 8H+ → 3Fe2+ + 2NO↑+ 4H2O (1)
0,075 ← 0,2 (mol)
=> Sau phản ứng (1) số mol Fe dư là 0,1 – 0,075 = 0,025 (mol)
Fe + Cu2+ → Fe2+ + Cu↓
0,025 → 0,025 → 0,025 (mol)
m↓ = mCu = 0,025.64 = 1,6 (g) => chọn A
Ghi nhớ: NO3- trong môi trường H+ có tính oxi hóa như axit HNO3
đáp án A
Ta có nFe = 0,1 || nCu(NO2)2 = 0,1 || nHCl = 0,24
● Nhận thấy nH+ = 0,24 và nNO3– = 0,2 ⇒ nNO = 0,06
● Ta có 3nNO > 2nFe ⇒ Fe chỉ lên Fe2+.
⇒ nFe phản ứng với HNO3 = nNO × 3 ÷ 2 = 0,09 mol
⇒ nFe phản ứng với Cu2+ = 0,1 - 0,09 = 0,01 mol
⇒ m↓ = mCu = 0,01×64 = 0,64 gam ⇒ Chọn A