Cho 8g hỗn hợp A gồm etanol và 2 Ancol đơn chức đồng đẳng cạnh nhau phản ứng với Na dư được 1,12 lít khí H2 đktc .Nếu đốt cháy hết 8g A cần vừa hết 0,65mol O2 và tạo ra a mol CO2 . Tìm a :
A. 0,25 mol
B. 0,4 mol
C. 0,5 mol
D. 0,45 mol
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{12,32}{22,4}=0,55\left(mol\right)\)
PT: \(R\left(OH\right)_x+xNa\rightarrow R\left(ONa\right)_x+\dfrac{x}{2}H_2\)
Theo PT: \(n_{R\left(OH\right)_x}=\dfrac{2}{x}n_{H_2}\Rightarrow0,5=\dfrac{2}{x}.0,55\Rightarrow x=2,2\) = số O
\(n_{CO_2}=\dfrac{12,32}{22,4}=0,55\left(mol\right)\)
⇒ Số C = \(\dfrac{0,55}{0,25}=2,2\)
→ Số C = số O nên hh X chỉ gồm ancol no.
⇒ nX = nH2O - nCO2 ⇒ nH2O = 0,8 (mol)
BTNT O, có: 2,2nX + 2nO2 = 2nCO2 + nH2O
⇒ nO2 = 0,675 (mol)
\(\Rightarrow V_{O_2}=0,675.22,4=15,12\left(l\right)\)

Chọn đáp án B
+ Xét 0,5 mol X ⇒ ∑nOH– = 2nH2
⇒ Với 0,25 mol X ⇒ ∑nOH– = 0,55 mol. ⇒ nO/X = 0,55 mol.
⇒ Nhận thấy nCO2 = nO = 0,55 mol
Vì số C = số Oxi ⇒ các ancol phải là các ancol no.
⇒ nAncol = nH2O – nCO2
⇒ nH2O = 0,25 + 0,55 = 0,8 mol
⇒ Bảo toàn O ⇒ nO2 = (0,55×2 + 0,8 – 0,55) ÷ 2 = 0,675 mol
⇒ VO2 = 0,675 × 22,4 = 15,12 lít ⇒ Chọn B

Chọn đáp án B
+ Xét 0,5 mol X ⇒ ∑nOH– = 2nH2
⇒ Với 0,25 mol X ⇒ ∑nOH– = 0,55 mol.
⇒ nO/X = 0,55 mol.
⇒ Nhận thấy nCO2 = nO = 0,55 mol
Vì số C = số Oxi
⇒ các ancol phải là các ancol no.
⇒ nAncol = nH2O – nCO2
⇒ nH2O = 0,25 + 0,55 = 0,8 mol
⇒ Bảo toàn O
⇒ nO2 = (0,55×2 + 0,8 – 0,55) ÷ 2 = 0,675 mol
⇒ VO2 = 0,675 × 22,4 = 15,12 lít

Đáp án A
Theo giả thiết, ta có :
![]()
⇒ X gồm 2 ancol no C x = n CO 2 n H 2 O - n CO 2 = 2 , 5
⇒ X gồm 2 ancol no , 2 chưa n O trong X = 2 . ( 0 , 35 a - 0 , 25 a ) ⏟ n X = 0 , 2 a
Theo bảo toàn nguyên tố C, H và bảo toàn electron, ta có :
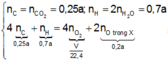
⇒ V = 7,28a
Lời giải:
nH2 = 0,05 ⇒ nOH- = nAncol = 0,05 .2 = 0,1
Đặt nH2O = b
Áp dụng định luật bảo toàn khối lượng có 18b + 44a = 8 + 0,65 .32 (1)
Áp dụng định luật bảo toàn O có:n O(H2O) + n O(CO2) = n O(A) + n O(O2)
⇒ b + 2a = 0,65 .2 + 0,1 (2)
Từ (1) và (2) ⇒ a = 0,45
Đáp án D.