Cho 2,24 gam bột sắt vào 200 ml dung dịch chúa hỗn hợp gồm AgNO3 0,1M và Cu(NO3)2 0,5M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y. Giá trị của m là
A. 2,80
B. 4,08
C. 2,16
D. 0,64
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C.
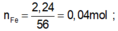
![]()
![]()
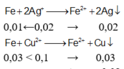
→ mrắn = mAg + mcu =0,02 . 108 + 0,03 . 64 = 4,08 (g)

nFe = 0,04 mol
nAg+ = 0,02 mol ; nCu2+ = 0,01 mol
Fe + 2Ag+ → Fe2+ + 2Ag
0,01 ← 0,02
Fe + Cu2+ → Fe2+ + Cu
0,03 0,1 → 0,03
Chất rắn sau phản ứng có : 0,02 mol Ag ; 0,03 mol Cu
=> m = 4,08g
Đáp án A

Chọn A
Vì: nFe = 0,04 mol
nAg+ = 0,02 mol ; nCu2+ = 0,01 mol
Fe + 2Ag+ → Fe2+ + 2Ag
0,01 ← 0,02
Fe + Cu2+ → Fe2+ + Cu
0,03 0,1 → 0,03
Chất rắn sau phản ứng có : 0,02 mol Ag ; 0,03 mol Cu
=> m = 4,08g

Chọn đáp án B
Ta có sơ đồ:
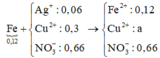
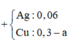
+ Rõ ràng AgNO3 đã phản ứng hết.
+ Ta có ∑nNO3– = 0,66 mol.
+ Bảo toàn điện tích ⇒ nCu2+ = (0,66 – 0,12x2) ÷ 2 = 0,21 mol.
⇒ nCu bị đẩy ra = 0,3 – 0,21 = 0,09 mol || nAg = 0,06 mol
⇒ mY = mCu + mAg = 0,06×108 + 0,09×64 = 12,24 gam
⇒ Chọn B
Chọn đáp án B