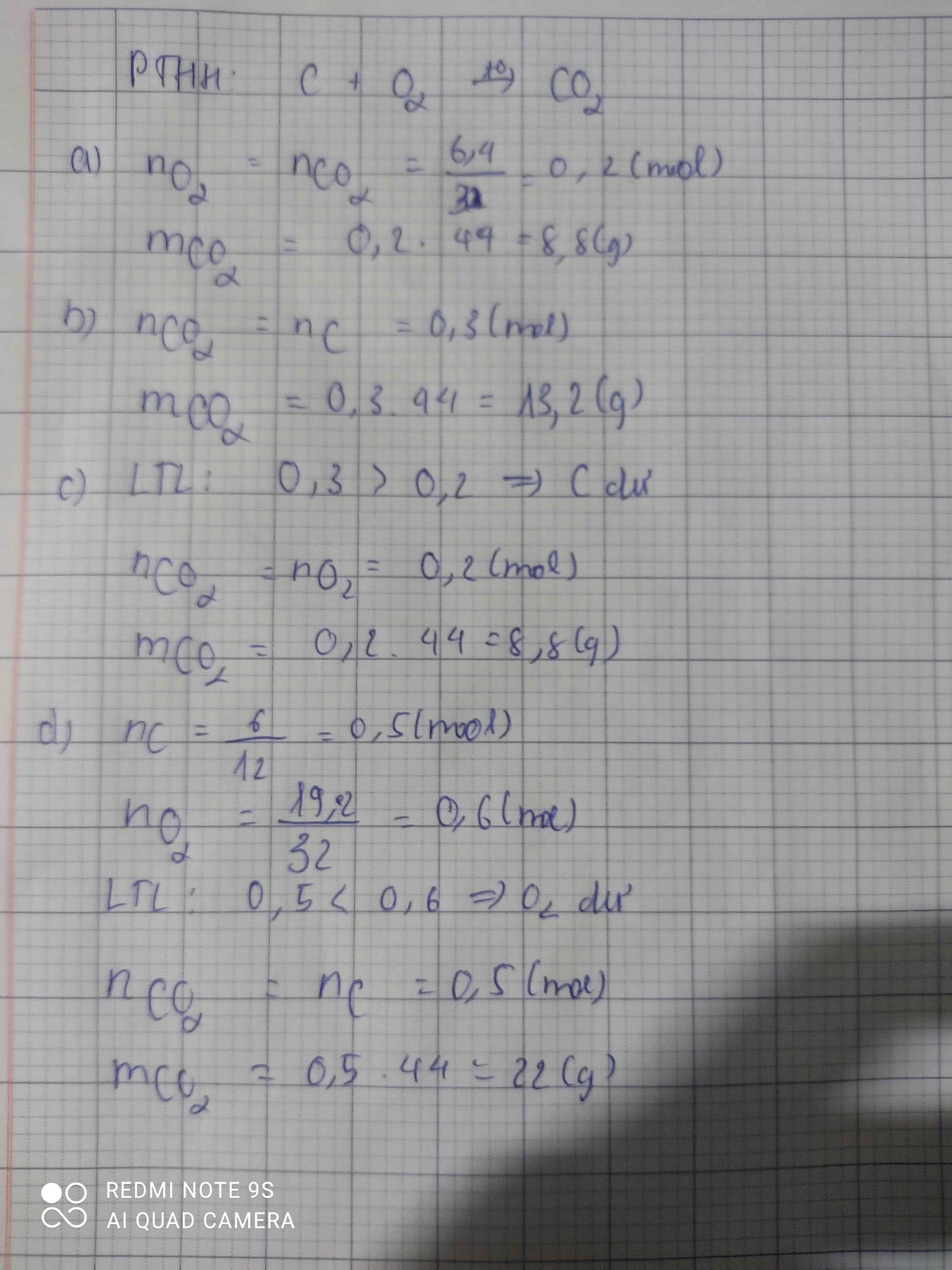Tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau: Khi đốt 0,3 mol cacbon trong bình chứa 4,48lit khí oxi ( đktc)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a)
C+O2-to>CO2
0,2---------0,2
nO2=0,2 mol
=>C dư
=>m CO2=0,2.44=8,8g
b) C+O2-to>CO2
0,5------------0,5 mol
n C=0,5 mol
n O2=0,6 mol
=>O2 dư
=>m CO2=0,5.44=22g
\(a,n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ PTHH:C+O_2\underrightarrow{t^o}CO_2\\ LTL:0,3>0,2\Rightarrow C.du\\ Theo.pt:n_{CO_2}=n_{O_2}=0,2\left(mol\right)\\ m_{CO_2}=0,2.44=8,8\left(g\right)\\ b,n_C=\dfrac{6}{12}=0,5\left(mol\right)\\ n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\ PTHH:C+O_2\underrightarrow{t^o}CO_2\\ LTL:0,5< 0,6\Rightarrow O_2.du\\ Theo.pt:n_{CO_2}=n_C=0,5\left(mol\right)\\ m_{CO_2}=0,5.44=22\left(g\right)\)

C + O2 -to-> CO2
a) nC= 0,3(mol)
nO2=0,2(mol)
Ta có: 0,3/1 > 0,2/1
=> C dư, O2 hết, tính theo nO2.
=> nCO2=nO2=0,2(mol)
=> mCO2= 0,2.44=8,8(l)
b) nC=0,5(mol); nO2=0,6(mol)
Ta có: 0,5/1 < 0,6/1
=> C hết, O2 dư, tính theo nC
=> nCO2=nC=0,5(mol)
=>mCO2=0,5.44=22(g)

Câu 1 :
\(2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ 2Mg + O_2 \xrightarrow{t^o} 2MgO\\ 2Cu + O_2 \xrightarrow{t^o} 2CuO\\ S + O_2 \xrightarrow{t^o} SO_2\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ C + O_2 \xrightarrow{t^o} CO_2\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\)

a)
\(C + O_2 \xrightarrow{t^o} CO_2\\ n_{CO_2} = n_{O_2} = \dfrac{6,4}{32} = 0,2(mol)\\ \Rightarrow m_{CO_2} = 0,2.44 = 8,8(gam)\)
b)
\(n_C = \dfrac{6}{12} = 0,5(mol)\\ n_{O_2} =\dfrac{19,2}{32} = 0,6(mol)\\ C + O_2 \xrightarrow{t^o} CO_2\)
\(n_C = 0,5 < n_{O_2} = 0,6 \Rightarrow\) Oxi dư.
\(n_{CO_2} = n_C = 0,5(mol)\\ \Rightarrow m_{CO_2} = 0,5.44 = 22(gam)\)

a) Viết phương trình hoá học của phản ứng đốt cháy cacbon trong oxi. Dựa vào phương trình hoá học và số liệu đề bài cho xem chất nào dư, chất nào tác dụng hết, tính thê tích khí CO2 theo chất tác dụng hết.
mCO2=8,8(g)mCO2=8,8(g)
b) Làm như hướng dẫn giải ở phần a : mCO2=22(g)mCO2=22(g).