Nhiệt phân 50,56 gam KMnO4 sau một thời gian thu được 46,72 gam chất rắn. Cho toàn bộ lượng khí sinh ra phản ứng hết với hỗn hợp X gồm Mg, Fe thu được hỗn hợp Y nặng 13,04 gam. Hòa tan hoàn toàn hỗn hợp Y trong dung dịch H2SO4 đặc nóng dư thu được 1,344 lít SO2 (đktc). % khối lượng Mg trong X là
A. 28,15%
B. 39,13%
C. 52,17%
D. 46,15%

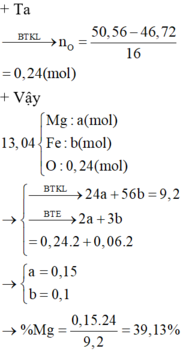
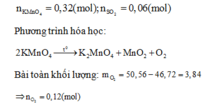
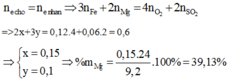
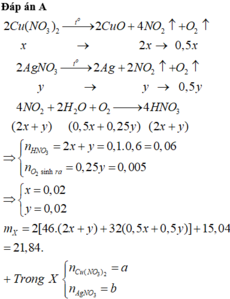

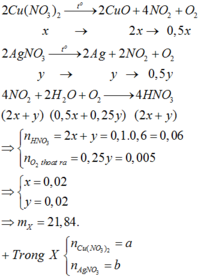
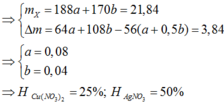
Đáp án B
B T K L : m O 2 = m K M n O 4 - m c r a n = 3 , 84 g ⇒ n O 2 = 0 , 12 m o l ⇒ n O = 0 , 24 m o l m M g , F e = m o x i t - m O = 13 , 04 - 0 , 24 . 16 = 9 , 2 g a m M g : x m o l F e : y m o l
⇒ % m M g = 39 , 13 %