Đốt cháy hoàn toàn một amin đơn chức bằng lượng không khí vừa đủ, chỉ thu được 0,15 mol C O 2 , 0,175 mol H 2 O và 0,975 mol N 2 ( b i ế t O 2 chiếm 20% thể tích không khí). Công thức phân tử của X là
A. C 3 H 7 N .
B. C 4 H 11 N .
C. C 3 H 9 N .
D. C 2 H 7 N .

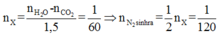
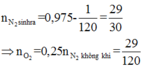
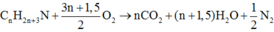
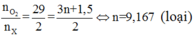
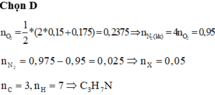


BTNT “O” ta có: 2 n O 2 = 2 n C O 2 + n H 2 O → n O 2 = 2.0 , 15 + 0 , 175 / 2 = 0 , 2375 m o l
Vì O2 chiếm 20% thể tích không khí còn lại là N2
→ nN2(trong kk) = 4.nO2 = 4. 0,2375 = 0,95 (mol)
→ nN2(sinh ra do đốt amin) = 0,975 – 0,95 = 0,025 (mol)
namin = 2 nN2(sinh ra do đốt amin) = 2.0,025 = 0,05 (mol)
Số C trong amin = nCO2/ namin = 0,15/0,05 = 3
Số H trong amin = 2nH2O/namin = 2.0,175/0,05 = 7
→ CTPT amin: C 3 H 7 N
Đáp án cần chọn là: A