Khi sục từ từ đến dư CO2 vào dung dịch hỗn hợp gồm a mol NaOH và b mol Ca(OH)2, kết quả thí nghiệm được biểu diễn trên đồ thị sau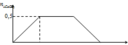
Tỉ lệ a : b là
A. 4 : 5
B. 5 : 4
C. 2 : 3
D. 4 : 3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
nCaCO3 max = nCa(OH)2 = b = 0,5 mol
nCO2 max = nNaHCO3 + 2nCa(HCO3)2
=> nNaHCO3 = nNaOH = a = 0,4 mol
=> a : b = 0,4 : 0,5 = 4 : 5

nCaCO3 max = nCa(OH)2 = b = 0,5 mol
nCO2 max = nNaHCO3 + 2nCa(HCO3)2
=> nNaHCO3 = nNaOH = a = 0,4 mol
=> a : b = 0,4 : 0,5 = 4 : 5
Đáp án A

Chọn đáp án A
Với mô hình đồ thị dạng này các bạn có thể hiểu là CO2 làm 3 nhiệm vụ như sau :
+ Nhiệm vụ 1 : Biến Ca(OH)2 thành kết tủa → b = 0,5 (mol)
+ Nhiệm vụ 2 : Biến NaOH thành NaHCO3 (đoạn chạy ngang)
+ Nhiệm vụ 3 : Hòa tan kết tủa
Vậy tổng của nhiệm vụ 2 và 3 ta có
![]()
![]()

Đáp án A
nCaCO3 max = nCa(OH)2 = b = 0,5 mol
nCO2 max = nNaHCO3 + 2nCa(HCO3)2
=> nNaHCO3 = nNaOH = a = 0,4 mol
=> a : b = 0,4 : 0,5 = 4 : 5

Đáp án A
+ Dựa vào giả thiết và bản chất phản ứng ta có đồ thị:
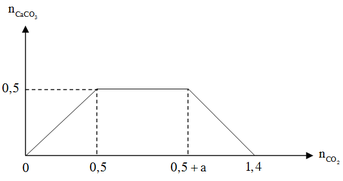
+ T a t h ấ y : b = 0 , 5 1 , 4 - ( 0 , 5 + a ) = 0 , 5 ⇒ b = 0 , 5 a = 0 , 4 ⇒ a b = 4 5

Đáp án A
nCaCO3 max = nCa(OH)2 = b = 0,5 mol
nCO2 max = nNaHCO3 + 2nCa(HCO3)2
=> nNaHCO3 = nNaOH = a = 0,4 mol
=> a : b = 0,4 : 0,5 = 4 : 5

Giải thích:
nCaCO3 max = nCa(OH)2 = b = 0,5 mol
nCO2 max = nNaHCO3 + 2nCa(HCO3)2
=> nNaHCO3 = nNaOH = a = 0,4 mol
=> a : b = 0,4 : 0,5 = 4 : 5
Đáp án A

Đáp án D
Đồ thị trải qua các giai đoạn :
+Kết tủa tăng dần do CO2 tác dụng với Ca(OH)2 → b = 0,4
+Kết tủa không đổi do CO2 tác dụng với NaOH tạo sản phẩm là Na2CO3 và sau đó là NaHCO3.
→ a = 0,9 - 0,4 = 0,5
+Kết tủa giảm dần do CO2 hòa tan kết tủa
→ a:b = 5:4

Đáp án D
Đồ thị trải qua các giai đoạn :
+Kết tủa tăng dần do CO2 tác dụng với Ca(OH)2 => b = 0,4
+Kết tủa không đổi do CO2 tác dụng với NaOH tạo sản phẩm là Na2CO3 và sau đó là NaHCO3.
=> a = 0,9 - 0,4 = 0,5
+Kết tủa giảm dần do CO2 hòa tan kết tủa
=> a:b = 5:4
Chọn đáp án A
Nhìn vào đồ thị ta thấy ngay b=0,5
Đoạn kết tủa chạy ngay là quá trình NaOH biến thành NaHCO3 nên a = 1,4 – 0,5 – 0,5 = 0,4(mol)