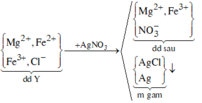
Cho 9,6 gam hỗn hợp gồm Mg và Fe có tỉ lệ mol 1:1 phản ứng với hỗn hợp khí X gồm Cl2 và O2, sau phản ứng chỉ thu được hỗn hợp rắn gồm các oxit và muối clorua, không còn khí dư. Hòa tan hoàn toàn hỗn hợp sản phẩm bằng một lượng vừa đủ 360ml dung dịch HCl 1M, thu được dung dịch Y. Cho AgNO3 dư vào dung dịch Y, thu được 85,035 gam kết tủa. Phần trăm thể tích của O2 trong hỗn hợp X là:
A. 48,18%
B. 23,3%
C. 46,15%
D. 43,64%


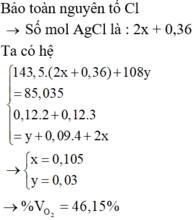

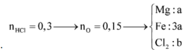
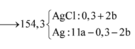
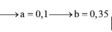
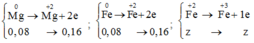
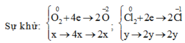
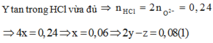
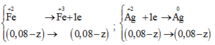
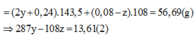
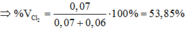
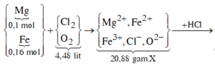
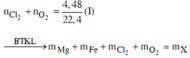
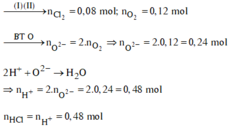
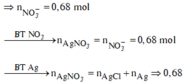


Đáp án C
nMg=nFe=9,6/(24+56)=0,12 mol
nO=nH+/2=0,36/2=0,18 mol => nO2=0,09 mol
nCl2=z
Giả sử trong Y:
Fe2+: x
Fe3+: y
Cl-: 2z+0,36 (BTNT Cl)
Fe2+ + Ag+ → Fe3+ + Ag
x x
Ag+ + Cl- → AgCl
2z+0,36 2z+0,36
BTNT Fe: x+y=0,12 (1)
BT e: 0,12.2+2x+3y=2z+0,18.2 (2)
m kết tủa = 108x+143,5(2z+0,36) = 85,035 (3)
Giải hệ pt ta được: x=0,03; y=0,09; z=0,105
%VO2=0,09/(0,09+0,105)=46,15%