Trong tự nhiên Oxi có 3 đồng vị 16O(x1%) , 17O(x2%) , 18O(4%), nguyên tử khối trung bình của Oxi là 16,14. Phần trăm đồng vị 16O và 17O lần lượt là
A. 35% & 61%
B. 90% & 6%
C. 80% & 16%
D. 25% & 71%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Ta có :
x1 + x2 + 4 = 100
A ¯ = 16 x 1 + 17 x 2 + 18 . 4 100 = 16 , 14
Vậy x1 = 90, x2 = 6

Đáp án B
• 16O : 17O = 4504 : 301; 18O : 17O = 585 : 903 = 195 : 301
→ 16O : 17O : 18O = 4504 : 301 : 195
Phần trăm từng đồng vị của O là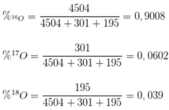
Khối lượng trung bình nguyên tử O là:
MO = 16 x 0,9008 + 17 x 0,0602 + 18 x 0,039 = 16,1382
nO = 752,875. 1020 : (1,6023. 1023) = 0,125 mol
→ mO = 0,125 x 16,1382 = 2,017275 gam

\(\overline{M}_O=\dfrac{16.99,76+17.0,039+18.0,201}{100}=16\left(g/mol\right)\)

Khi có 1 nguyên tử 17O, mà % nguyên tử của 17O = 0,039%
⇒ Số nguyên tử O = 1 : 0,039% = 2564 nguyên tử
99,757% 16O ⇒ Số nguyên tử 16O = 99,757%.2564 = 2558 nguyên tử
0,204% 18O ⇒ Số nguyên tử 18O = 0,204%.2564 = 5 nguyên tử

\(\overline{M}=\dfrac{99,757.16+0,039.17+0,204.18}{100}=16,004\left(g/mol\right)\)
=> D

Đáp án B
Phân tử khối của NO2 nằm trong khoảng:
14 + 16 + 16 ≤ MNO2 ≤ 15 + 18 + 18
→ 46 ≤ MNO2 ≤ 51
Vậy có 6 giá trị phân tử khối của NO2 là 46, 47, 48, 49, 50, 51
Đáp án B
Luôn có x1 + x2 + 4 = 100 (1)
Nguyên tử khối trung bình của O là
16 , 4 = ( 16 x 1 + 17 x 2 + 18 . 4 ) / 100 (2)
Từ (1) và (2) => x 1 = 90 ; x 2 = 6