Đốt cháy hết 9,18 gam 2 đồng đẳng của benzen A, B thu được 8,1 gam H2O và V lít CO2 (đktc). Giá trị của V là :
A. 15,465.
B. 15,456.
C. 15,546.
D. 15,654.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt công thức phân tử trung bình của
A và B là : C n ¯ H 2 n ¯ − 6
Theo giả thiết ta có :
n H 2 O = 8 , 1 18 = 0 , 45 m o l ⇒ m H = 0 , 45.2 = 0 , 9 g a m ⇒ m C = 9 , 18 − 0 , 9 = 8 , 28 g a m n C O 2 = n C = 8 , 28 12 = 0 , 69 m o l .
Vậy thể tích CO2 thu được là : 0,69.22,4=15,456 lít.

Đáp án C
Hướng dẫn mC = 9,18 – 0,45.2 = 8,28 gam; nCO2 = 0,69 mol; T = 0,1/0,69 = 0,14
=> tạo muối NaHCO3
mNaHCO3 = 0,1. 84 = 8,4 g

Đáp án B
Hướng dẫn
Đặt công thức phân tử trung bình của A và B là : C n ¯ H 2 n ¯ − 6 .
Phương trình phản ứng :
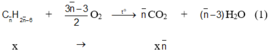
Theo (1) và giả thiết ta có : ( 14 n ¯ − 6 ) x = 9 , 18 n ¯ x = 0 , 69 ⇒ n ¯ = 8 , 625 x = 0 , 08
Vậy Công thức phân tử của A và B lần lượt là C8H10 và C9H12

Đáp án : B
nCO2 = 0,69 mol => nC = 0,69 => nH = 9,18 - 0,69 . 12 = 0,9
Đặt công thức chung của A và B là CnH2n - 6, ta có:
n / (2n - 6) = 0,69/0,9 => n = 8,625
=> 2 hidocacbon đó là C8H10 ; C9H12

Đáp án : B
nCO2 = 0,69 mol => nC = 0,69 => nH = 9,18 - 0,69 . 12 = 0,9
Đặt công thức chung của A và B là CnH2n - 6, ta có:
n / (2n - 6) = 0,69/0,9 => n = 8,625
=> 2 hidocacbon đó là C8H10 ; C9H12

Đáp án A
Hướng dẫn nCO2 = 7,728/ 22,4 = 0,345 mol; nH2O = 4,05/18 = 0,225 => m = mC + mH = 0,345.12 + 0,225.2 = 4,59 g; n = (0,345 – 0,225)/3 = 0,04 mol

Chọn đáp án D
Vì n C O 2 = n H 2 O = 1 , 3 m o l ⇒ Cả 3 este đều có dạng CnH2nO2
BTTN (O) ⇒ n O 2 = 1 , 3 × 2 + 1 , 3 - 0 , 4 × 2 2 = 1 , 55 m o l
Đáp án B