Khi nhỏ từ từ đến dư dung dịch NaOH vào dung dịch hỗn hợp gồm AlCl3 và FeCl3, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
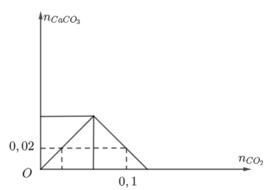
Khi x = 0,66 thì giá trị của m (gam) là?
A. 12,14
B. 14,80
C. 11,79
D. 12,66
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D.
x = 0,6 mol thì kết tủa cực đại
⇒ 3 n F e C l 3 + 3 n A l C l 3 = 0 , 6 m o l
x = 0,74 mol thì kết tủa bị hòa tan nhiều nhất
⇒ n A l ( O H ) 3 = 0 , 74 - 0 , 6 = 0 , 14 m o l ⇒ n A l C l 3 = 0 , 14 m o l , n F e C L 3 = 0 , 06 m o l
x = 0,66 mol thì kết tủa bị hòa tan một phần:
n A l ( O H ) 3 b ị h ò a tan = 0 , 66 - 0 , 6 = 0 , 06 m o l ⇒ m = m A l ( O H ) 3 d ư + m F e ( O H ) 3 = 78 ( 0 , 14 - 0 , 06 ) + 107 . 0 , 06 = 12 , 66 g a m

Giải thích:
Tại nNaOH = 0,8 mol thì bắt đầu có kết tủa xuất hiện
⇒ H+ trung hòa vừa hết ⇒ nHCl = a = 0,8 mol
Tại nNaOH = 2,0 và 2,8 mol thì cùng thu được lượng kết tủa như nhau
+) nNaOH = 2,0 mol thì Al3+ dư
+) nNaOH = 2,8 mol thì kết tủa tan 1 phần:
nAl(OH)3 = 4nAl3+−(nOH − nHCl) ⇒ nAlCl3 = b = 0,6 mol
Đáp án B


b.
3NaOH + FeCl3 → 3NaCl + Fe(OH)3↓
0,24 ← 0,08 → 0,08
3NaOH + AlCl3 → 3NaCl + Al(OH)3↓
0,42 ← 0,14 → 0,14
Sau pứ: nNaOHdư = 0,74 – (0,24 + 0,42) = 0,08
NaOH + Al(OH)3 → NaAlO2 + 2H2O
0,08 → 0,08
Dư: 0,06
Suy ra m↓ = mFe(OH)3 + mAl(OH)3 = 0,08 . 107 + 0,06 . 78 = 13,24g

Đáp án B.
![]()
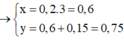
=> x:y = 4:5
CH2=CH-C≡CH + H2 → Pd , PbCO 3 H 2 , t o CH2=CH-CH=CH2
nCH2=CH-CH=CH2 + nCH2=CH-CN → xt , p t o (-CH2-CH=CH-CH2-CH2-CH(CN)-)n.
Đáp án D