Phản ứng được dùng để điều chế Br2 trong công nghiệp là
A. 2AgBr → 2Ag + Br2
B. 2HBr + Cl2 → 2HCl + Br2
C. 2NaBr + Cl2 → 2NaCl + Br2
D. 2H2SO4 + 4KBr + MnO2 → 2K2SO4 + MnBr2 + Br2 + 2H2O
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
Các phản ứng có sự thay đổi số oxi hóa của các nguyên tố là phản ứng oxi hóa khử.Gồm:
1,3,5,6

Vai trò các chất trong các phản ứng oxi hóa – khử sau là:
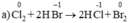
Chất khử 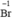 (trong HBr), chất oxi hóa Cl2
(trong HBr), chất oxi hóa Cl2
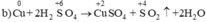
Chất khử Cu, chất oxi hóa 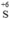 (trong H2SO4)
(trong H2SO4)
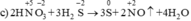
Chất khử 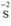 (trong H2S), chất oxi hóa
(trong H2S), chất oxi hóa 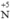 (trong HNO3)
(trong HNO3)
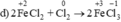
Chất khử 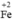 (trong FeCl2), chất oxi hóa
(trong FeCl2), chất oxi hóa 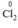

Đáp án C
Các phương trình viết đúng là:
(1). Cl2 + 2NaBr → 2NaCl + Br2
(2). Br2 + 2NaI → 2NaBr + I2
(7). HCl + AgNO3 → AgCl + HNO3
(4). Br2 + 5Cl2 + 6H2O → 2HBrO3 + 10HCl
(8). PBr3 + 3H2O → H3PO3 + 3HBr
Các phản ứng viết sai là:
(3). Cl2 + 2NaF → 2NaCl + F2 vì tính oxi hóa của Cl2 yếu hơn Flo.
(5). F2 + 2NaCl → 2NaF + Cl2 vì Flo có tính oxi hóa rất mạnh nó oxi hóa được H2O.
(6). HF + AgNO3 → AgF + HNO3 vì AgF là chất tan.

Đáp án D.
Phản ứng oxi hóa khử xảy ra theo chiều:
Chất oxi hóa mạnh + chất khử mạnh → Chất oxi hóa yếu hơn + chất khử yếu hơn
ü Phản ứng 2FeBr2 + Br2 → 2FeBr3
→ Tính oxi hóa của Br2 mạnh hơn F e 3 + (1)
ü Phản ứng 2NaBr + Cl2 → 2NaCl + Br2
→ Tính oxi hóa của Cl2 mạnh hơn Br2(2)
Từ (1) và (2) → Cl2 có tính oxi hóa mạnh hơn F e 3 +
Trong công nghiệp, sau khi lấy muối ăn từ nước biển, phần còn lại chứa nhiều muối brom của natri và kali, người ta sục khí clo qua dung dịch muối đó sẽ thu được brom