Một lượng khí khối lượng 15 kg chứa 5,64. 10 26 phân tử. Phân tử khí này gồm các nguyên tử hiđrô và cacbon. Hãy xác định khối lượng của nguyên cacbon và hiđrô trong khí này. Biết 1 mol khí có N A = 6,02. 10 23 phân tử.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án: D
Gọi M - khối lượng mol phân tử của chất khí
Ta có, số mol khí bằng: n = m M = N N A
Với N = 11,28.10 26 N A = 6,02.10 23 m = 30 k g = 30.10 3 g
Ta suy ra: M = m N A N = 30.10 3 .6,02.10 23 11,28.10 26 = 16 g / m o l
Mặt khác, phân tử khí này gồm các nguyên tử hiđro và cacbon
Khí CH4 có khối lượng mol phân tử là M = 12 + 4 = 16 g / m o l
=> Khí đã cho là C H 4

\(N=\dfrac{M}{300}=\dfrac{9.10^5}{300}=3000\left(Nu\right)\\L=\dfrac{N}{2}.3,4=\dfrac{3000}{2}.3,4=5100\left(A^o\right)\\ Ta.có:\left\{{}\begin{matrix}\%A+\%G=50\%N=1500\left(Nu\right)\\\%A-\%G=10\%N=300\left(Nu\right)\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}A=T=900\left(Nu\right)\\G=X=600\left(Nu\right)\end{matrix}\right.\\ H=2A+3G=2.900+3.600=3600\left(liên.kết\right)\)

B
Khối lượng 1 phân tử nước m 0 = 2 . 1 , 67 . 10 - 27 + 26 , 56 . 10 - 27 = 29 , 9 . 10 - 27 kg
Số phân tử nước trong 1 gam nước
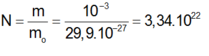

Đặt CTHH của hợp chất CzHy
Ta có:
IV x z=I x y nên x/y=I/IV=1/4
Vậy hợp chất trên có dạng CH4.
Trong 1 mol CH4 có 6x10^23 nguyên tử C và 2,4x10^24 nguyên tử H.

Gọi công thức hóa học của hợp chất là CxHy
Ta có : Cacbon chiếm 82,76% nên Hidro chiếm 17,24%
Ta có : \(\frac{12x}{82,76}=\frac{y}{17,24}=\frac{12x+y}{82,76+17,24}=\frac{58}{100}=0,58\)
\(\Rightarrow\frac{12x}{82,76}=0,58\Rightarrow x=4\)
\(\Rightarrow\frac{y}{17,24}=0,58\Rightarrow y=10\)
Vậy CTHH CxHy là C4H10
Vậy có 4C và 10H

\(\%C = \dfrac{12x}{12x + y}.100\% = 82,76\%\\ \Rightarrow 2,5x = y(1)\)
Ta có :
\(M_A = \dfrac{2.16 + 1.(12x + y)}{2 + 1} = 7,5.4\\ \Rightarrow 12x + y = 58(2)\)
Từ (1)(2) suy ra x = 4 ; y = 10
Vậy CTPT của hợp chất cần tìm : C4H10
2.5x=y
12x+y=58
Thì mình bấm giải hệ phuong trình trên máy tính sao a

a/Gọi CTPT của khí trên là CxOy
Ta có: mC=\(\frac{12x}{12x+16y}\) mO=\(\frac{16y}{12x+16y}\)
Lại có: mC / mO = 3 / 8
<=> \(\frac{12x}{16y}\) = \(\frac{3}{8}\)
=> \(\frac{x}{y}\) = \(\frac{1}{2}\)
=> CTPT: CO2
b/Giải thích:-Hiệu ứng nhà kính là hiệu ứng làm cho không khí của Trái đất nóng lên do bức xạ sóng ngắn của Mặt trời có thể xuyên qua tầng khí quyển chiếu xuống mặt đất; mặt đất hấp thu nóng lên lại bức xạ sóng dài vào khí quyển để CO2 hấp thu làm cho không khí nóng lên. CO2 trong khí quyển giống như một tầng kính dày bao phủ Trái đất, làm cho Trái đất không khác gì một nhà kính lớn
-Cùng với sự phát triển dân số và công nghiệp với tốc độ cao, CO2 thải vào khí quyển cũng tăng theo. Rừng lại bị chặt phá quá mức, CO2 đáng lẽ được rừng cây hấp thu lại không được hấp thu, nên lượng CO2 ngày càng tăng, hiệu ứng nhà kính do đó tăng theo không ngừng.
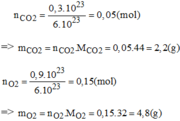
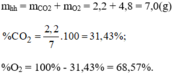
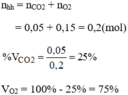
Số mol khí: n = N/ N A (N là số phân tử khí)
Mặt khác n = m/ μ . Do đó: μ = m N A /N = 15.6,02. 10 23 /5,46. 10 26 = 16,01. 10 - 3 (kg/mol) (1)
Trong các khí có hidro và cacbon thì C H 4 có:
μ = (12 + 4). 10 - 3 kg/mol (2)
So sánh (2) với (1) ta thấy phù hợp. Vậy khí đã cho là C H 4
Khối lượng của phân tử hợp chất là: m C H 4 = m/N
Khối lượng của nguyên tử hidro là:
m H 4 = 4/16 . m C H 4 = 4/16 . m/N ≈ 6,64. 10 - 27 (kg)
Khối lượng nguyên tử cacbon là:
m C = 12/16 . m C H 4 = 12/16 . m/N ≈ = 2. 10 - 26 (kg)