Người ta dùng khí cacbon oxit để khử đồng (II) oxit. Cho a = 150g, hãy tính kết quả bằng số.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) nCu=0,2(mol)
PTHH: CuO + H2 -to-> Cu + H2O
b) nH2=nCuO=nCu=0,2(mol)
=>V(H2,đktc)=0,2.22,4=4,48(l)
c) mCuO=0,2.80=16(g)

1)
\(C+H_2O\underrightarrow{t^O}CO+H_2\) (1)
\(C+2H_2O\underrightarrow{t^o}CO_2+2H_2\) (2)
2)
Gọi số mol CO, CO2 là a, b (mol)
\(n_{H_2\left(1\right)}=n_{CO}=a\left(mol\right)\)
\(n_{H_2\left(2\right)}=2b\left(mol\right)\)
=> \(n_{H_2}=a+2b\left(mol\right)\)
=> a + b + (a+2b) = \(\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
=> 2a + 3b = 0,5
PTHH: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(CuO+CO\underrightarrow{t^o}Cu+CO_2\)
=> \(n_{H_2}+n_{CO}=n_{Cu}=\dfrac{25,6}{64}=0,4\)
=> (a + 2b) + a = 0,4
=> 2a + 2b = 0,4
=> a = 0,1 ; b = 0,1
=> X chứa \(\left\{{}\begin{matrix}CO:0,1\left(mol\right)\\CO_2:0,1\left(mol\right)\\H_2:0,3\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,1}{0,5}.100\%=20\%\\\%V_{CO_2}=\dfrac{0,1}{0,5}.100\%=20\%\\\%V_{H_2}=\dfrac{0,3}{0,5}.100\%=60\%\end{matrix}\right.\)
\(\overline{M}_X=\dfrac{0,1.28+0,1.44+0,3.2}{0,5}=15,6\left(g/mol\right)\)
=> \(d_{X/O_2}=\dfrac{15,6}{32}=0,4875\)

1. C + H2O \(\underrightarrow{t^o}\) CO + H2
C + 2H2O \(\underrightarrow{t^o}\) CO2 + 2H2.
2. Lượng Cu thu được là 0,4 mol, suy ra lượng đồng (II) oxit phản ứng là 0,4 mol. Lượng nguyên tử oxi phản ứng là 0,4 mol.
Suy ra, tổng lượng CO và H2 trong X là 0,4 mol. Lượng khí X là 0,5 mol. Suy ra, số mol CO2 là 0,1 mol.
Gọi a mol và b mol lần lượt là số mol của CO và H2 có trong X.
Lượng C và H2O ban đầu lần lượt là (0,1+a) mol và b mol.
BTKL: 12(0,1+a)+18b=28a+2b+44.0,1 (1)
a+b=0,4 (2).
Từ (1) và (2), suy ra a=0,1 và b=0,3.
Tỉ lệ phần trăm thể tích các khí có trong X:
%VCO=0,1/0,5=20%, %\(V_{H_2}\)=0,3/0,5=60%, %\(V_{CO_2}\)=20%.
Phân tử khối trung bình của X là (28.0,1+2.0,3+44.0,1)/0,5=7,6.
Tỉ khối của X so với oxi là dX/O=7,6/16=0,475.

nCuO = 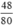 = 0,6 mol.
= 0,6 mol.
Phương trình hóa học của phản ứng khử CuO:
CuO + H2 → Cu + H2O.
nCu = 0,6mol.
mCu = 0,6 .64 = 38,4g.
Theo phương trình phản ứng trên:
nH2 = 0,6 mol
VH2 = 0,6 .22,4 = 13,44 lít.

\(n_{H_2}=\dfrac{0,65}{22,4}=0,029mol\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,29 0,29 0,29 ( mol )
\(m_{Cu}=0,29.64=18,56g\)
\(m_{CuO}=0,29.80=23,2g\)

PTHH: CuO + H2 → Cu + H2O
Số mol của Cu là: 24 : 64 = 0,375 (mol)
Số mol của H2 là: 0,375 mol
Thể tích hiđrô đã dùng là: 0,375 . 22,4 = 8,4 lít
Số mol của CuO là: 0,375 mol
Khối lượng CuO bị khử là: 0,375 . 80 = 30 gam
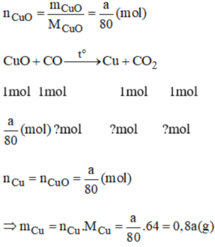

a = 150g
⇒ m C u = 0,8a = 0,8.150 = 120(g)