Cho 5,6 lít CO2 đktc hấp thụ hết vào 500 ml dung dịch hỗn hợp NaOH 0,15 M và Ba(OH)2 0,3 M, thu được m gam kết tủa. Giá trị của m là
A. 14,775 gam
B. 49,250 gam
C. 24,625 gam
D. 12,500 gam
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Theo bảo toàn electron, ta có :
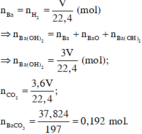
Ta có đồ thị :
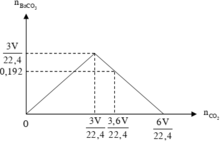
Căn cứ vào tính chất của đồ thị, suy ra :
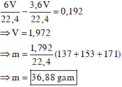

Đáp án C
n CO2 = 0,4 mol , n KOH = 0,12 mol , n Ba(OH)2 = 0,24 mol
=> n OH- = 0,24 .2 + 0,12 = 0,6 mol
CO2 + OH- → HCO3-
0,4 0,6 => 0,4 , n OH-dư = 0,2 mol
HCO3- + OH-→ CO32- + H2O
0,4 0,2 => 0,2 mol , dư HCO3-
Ba2+ + CO32- → BaCO3
0,24 0,2 => 0,2 mol
=> m BaCO3 = 39,4 g

nNaOH = nBa(OH)2 = 0,1
→ n O H - = 0,3
nCO2 = 0,2—> nCO32- = nHCO3- = 0,1
—> nBaCO3 = 0,1
—> mBaCO3 = 19,7 gam
Đáp án D

Chọn D
Ta có: T = n O H - n C O 2 = 0 , 03 0 , 02 = 1 , 5 . Do đó có các quá trình sau xảy ra:
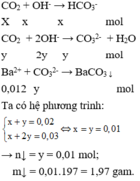
Đáp án C
nCO2 = 0,25 mol
nOH- = 0,5.0,15 + 0,3.2.0,5 = 0,375 mol
→ tạo cả HCO3- : x mol và CO32- : y mol
Bảo toàn C có 0,25 = x + y
Bảo toàn điện tích có x + 2y = 0,5.0,15 + 0,5.0,3.2
→ x = y = 0,125 mol
Ba2+ + CO32- → BaCO3
→nBaCO3 = 0,125.197=24,625 g