Nguyên tử của nguyên tố X có tổng số hạt mang điện trong hạt nhân là 13. Vị trí của X trong bảng tuần hoàn là
A. Chu kỳ 3, nhóm IIIA.
B. Chu kỳ 2, nhóm IIIA.
C. Chu kỳ 3, nhóm IIA.
D. Chu kỳ 3, nhóm VIIA.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo đề bài ta có : 2Z + N = 40
N ≥ Z . Vì vậy ta có : 3Z ≥ 40, do đó Z ≤ 40/3 = 13,3 (1)
Măt khác : N/Z ≤ 1,5 → N ≤ 1,5Z
Từ đó ta có : 2Z + N ≤ 2Z + 1,5Z; 40 ≤ 3,5Z
→ Z ≥ 40/3,5 = 11,4 (2)
Tổ hợp (1) và (2) ta có : 11,4 ≤ Z ≤ 13,3 mà z nguyên. Vậy Z= 12 và Z = 13.
Nếu Z = 12 thì N = 16 và A = 28 (trái với đề bài A < 28)
Vậy Z = 13. Đó là nguyên tố nhôm (Al).
Vị trí của nhôm trong bảng tuần hoàn :
+ Ô số 13 ;
+ Chu kì 3 ;
+ Nhóm IIIA.

Cái này chắc hóa 7 không vậy fen=))
C16:
\(2p+12=24\Rightarrow p=6:Cacbon:1s^22s^22p^2\)
Chu kì 2, nhóm IVA, là phi kim (có 4 e hóa trị lớp ngoài cùng)
Đề cho đáp án sai, sure=0
C17: B
C18: \(\%K=\dfrac{39.100}{39+14+16.3}=38,61\%\)
Chọn A
C19: \(p+12=24\Rightarrow p=12\) => ô 12
Chọn A
C20: liên kết ion
Liên kết ion của 2 nguyên tử trong 1 phân tử là lấy giá trị tuyệt đối của hiệu độ âm điện của 2 nguyên tử tính ra lớn hoặc bằng 1,7.

Đáp án D
Hai nguyên tố thuộc cùng một nhóm A, thuộc hai chu kỳ liên tiếp = Điện tích hạt nhân cách nhau 8, 18 hay 32
Trường hợp 1:
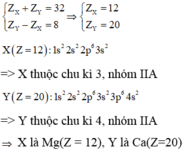
Trường hợp 2:
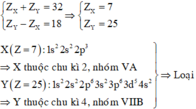
Trường hợp 3:
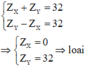

Vì 2 nguyên tố X, Y thuộc 2 nhóm A liên tiếp nên: \(\left\{{}\begin{matrix}Z_X+Z_Y=39\\Z_Y-Z_X=1\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}Z_X=19\\Z_Y=20\end{matrix}\right.\)
ZX=19 => Cấu hình e: \(1s^22s^22p^63s^23p^64s^1\)
=> X thuộc ô 19 là Kali (K), nhóm IA, chu kỳ IV
ZX=20 => Cấu hình e: \(1s^22s^22p^63s^23p^64s^2\)
=> X thuộc ô 20 là Canxi (Ca), nhóm IIA, chu kỳ IV

Zx+zy=51
Hai nhóm liên kết nhau ở chu kỳ 4
=> TH1: zy-zx=1
=>TH2: zy-zx=11

Chọn B
Số lớp electron của X bằng số thứ tự chu kỳ và bằng 3.
Đáp án đúng : A